
Clinical Questions
CQ 2:IBD関連消化管腫瘍のリスク因子は?
CQ 3:IBD関連消化管腫瘍の臨床病理学的特徴は,日本人と欧米人との間に違いはあるか?
CQ 4:IBDに対する薬物療法は関連消化管腫瘍発生リスクに影響するか?
CQ 5:IBD関連消化管腫瘍に対する内視鏡によるサーベイランスは有効か?
CQ 6:サーベイランスにおける最適な内視鏡検査の方法(開始時期,施行間隔,観察方法など)は何か?
CQ 7:IBD関連消化管腫瘍に対する内視鏡検査以外のサーベイランスは有効か?
CQ 8:大腸内視鏡検査によるサーベイランスにおける最適な生検方法は何か?
CQ 9:CD関連直腸肛門管癌の診断に麻酔下肛門部観察(examination under anesthesia:EUA)は推奨されるか?
CQ 10:UC関連大腸腫瘍とsporadic colorectal neoplasia(散発性大腸腫瘍)の鑑別となる内視鏡所見は何か?
CQ 11:IBD関連消化管腫瘍に用いるべき病理診断用語・分類・基準は何か?
CQ 12:IBD関連消化管腫瘍の生検病理診断において免疫染色(p53,Ki-67)は推奨されるか?
CQ 13:IBD関連消化管腫瘍と散発性腫瘍の病理所見の違いは何か?
CQ 14:UC関連大腸腫瘍に対して大腸全摘術は推奨されるか?
CQ 15:CD関連大腸腫瘍に対して大腸部分切除は推奨されるか?
CQ 16:UC関連大腸腫瘍に対する括約筋温存手術として回腸囊肛門吻合術(ileoanal anastomosis:IAA)は推奨されるか?
CQ 17:UC関連直腸癌に対して括約筋温存手術は推奨されるか?
CQ 18:CD関連直腸肛門管癌に対する最適な術式は何か?
CQ 19:CD関連小腸癌に対する最適な術式は何か?
CQ 20:IBD関連消化管癌に対する低侵襲手術は推奨されるか?
CQ 21:UC関連大腸腫瘍に対して内視鏡切除は推奨されるか?
CQ 22:UC関連大腸腫瘍に対する内視鏡切除後の最適なサーベイランス法は何か?
CQ 23:IBD関連消化管癌手術後のIBD薬物治療の注意点は何か?
CQ 24:IBD関連消化管腫瘍手術後の補助化学療法は推奨されるか?
CQ 25:IBD関連の進行・再発消化管癌に対する薬物療法は推奨されるか?
CQ 26:IBD関連直腸癌に対する術前化学放射線療法は有効か?
CQ 27:IBD関連消化管癌は散発性消化管癌と比較して予後不良か?
CQ 28:IBD患者に消化管以外の腫瘍発生リスクはあるか?
CQ 1:IBD関連消化管腫瘍の定義は何か?
IBDの炎症粘膜に発生した上皮性腫瘍で,病理学的に散発性腫瘍と診断される腫瘍を除いたもの。
● 解説
UCやCD(以下IBD)では,発症から8~10年で大腸および小腸癌の発生頻度が一般人口に比べ有意に高率になるとされている1-3)。こうした慢性持続性炎症粘膜における発癌は炎症性発癌と呼ばれている4)。炎症性発癌の前段階には,IBDの慢性持続性炎症を背景とした,細菌・ウイルスなどの感染因子,腸内細菌叢の変動,TNF-α,IL-6等の炎症性サイトカインや活性酸素・窒素などの内因性メディエイターによる種々の腫瘍関連遺伝子の変化やDNAのメチル化などのepigeneticな変化,炎症の酸化ストレスによるDNA傷害など,多岐にわたる因子が存在していることが考えられている5,6)。炎症性発癌はdysplasia7)と呼ばれる上皮内腫瘍を形態学的初期病変とすると考えられ,inflammation-dysplasia-carcinoma sequenceとも呼ばれている8)。
他方,IBDの腸管粘膜にも炎症とは無関係に腫瘍が発生する可能性もあるsporadic neoplasia(散発性腫瘍)。特に病悩期間が短期の場合や高齢者では,炎症性発癌とは異なる機序で発生したde novo癌,鋸歯状病変とその癌化例,腺腫(sporadic adenoma)とその癌化例(sporadic carcinoma)が含まれる可能性がある。IBD関連消化管腫瘍は,厳密には炎症粘膜を発生母地とする腫瘍(炎症性発癌)に限定して用いられるべきである。しかし,炎症性発癌病変の具体的判定基準は存在せず,IBDの炎症粘膜に発生した腫瘍はすべてIBD関連消化管腫瘍として扱われてきた。1990年代以降は,IBDの炎症罹患粘膜に発生した隆起性粘膜内腫瘍については,炎症性発癌病変か散発性腺腫かの区別がなされるようになってきた9,10)が,粘膜下層以深浸潤癌については炎症性発癌か散発性かの区別は未だなされていない11)。
IBD関連消化管腫瘍とは,炎症粘膜を発生母地とする腫瘍に限定して用いられるべき用語である。しかし,上述した理由から,現時点では“IBD関連消化管腫瘍とは,IBDの炎症粘膜に発生したすべての腫瘍の中で,病理学的に散発性粘膜内腫瘍と診断される病変を除いたもの”(散発性腫瘍の病理学的判断所見についてはCQ 13を参照)と定義するのが現実的と考えられる。しかし,今後の臨床および基礎的研究により,この定義が変動する可能性もある。特に,散発性鋸歯状病変やその癌化例の臨床的取り扱いが今後の課題の一つであろう。
ここで注意を要する点は,日本と欧米では粘膜内腫瘍に関する病理診断基準が異なり,欧米では粘膜内腫瘍に対しては原則として癌の診断を行わないことである12)。すなわち,欧米の研究,文献における癌とは粘膜下層以深に浸潤した上皮性腫瘍に対してのみ用いられ,粘膜内腫瘍はすべて腺腫もしくはdysplasiaと診断される。他方,日本の病理診断では,粘膜内腫瘍であってもその組織異型度から癌(粘膜内癌)の診断が行われる。このことから,欧米のsporadic adenomaの中には,日本の病理診断基準では腺腫内癌や純粋癌(腺腫非併存癌)と診断される病変が含まれている。
文献
- Harpaz N, Talbot IC:Colorectal cancer in idiopathic inflammatory bowel disease. Semin Diagn Pathol 1996;13:339-357
- Bernstein CN, Blanchard JF, Kliewer E, et al.:Cancer risk in patients with inflammatory bowel disease:a population-based study. Cancer 2001;91:854-862
- Eaden JA, Abrams KR, Mayberry JF:The risk of colorectal cancer in ulcerative colitis:a meta-analysis. Gut 2001;48:526-535
- Itzkowitz SH, Yio X:Inflammation and Cancer Ⅳ. Colorectal cancer in inflammatory bowel disease:the role of inflammation. Am J Physiol Gastrointest Liver Physiol 2004;287:G7-G17
- Ullman TA, Itzkowitz SH:Intestinal inflammation and cancer. Gastroenterology 2011;140:1807-1816
- Saraggi D, Fassan M, Mescoli C, et al.:The molecular landscape of colitis-associated carcinogenesis. Dig Liver Dis 2017;49:326-330
- Riddell RB, Goldman H, Ransohoff DF, et al.:Dysplasia in inflammatory bowel disease:standardized classification with provisional clinical applications. Hum Pathol 1983;14:931-968
- Velayos FS, Loftus EV Jr, Jess T, et al.:Predictive and protective factors associated with colorectal cancer in ulcerative colitis:a case-control study. Gastroenterology 2006;130:1941-1949
- Schneider A, Stolte M:Differential diagnosis of adenomas and dysplastic lesions in patient with ulcerative colitis. Z Gastroenterol 1993;31:653-656
- Odze RD:Adenomas and adenoma-like DALMs in chronic ulcerative colitis:a clinical, pathological, and molecular review. Am J Gastroenterol 1999;94:1746-1750
- Vieth M, Neumann H:Current issues in inflammatory bowel disease neoplasia. Histopathology 2015;66:37-48
- Odze RD, Riddell RH, Bosman FT, et al.:Premalignant lesions of the digestive system. In:Bosman FT, Carneiro F, Hruban RH, et al.:WHO Classification of Tumours of the Digestive System(4th ed), IARC, Lyon, 2010:10-12
CQ 2:IBD関連消化管腫瘍のリスク因子は?
UC関連大腸腫瘍
- 罹病期間,全大腸炎型,活動性炎症,炎症性ポリープ,PSCの合併,大腸癌家族歴が大腸癌発生のリスク因子である。(エビデンスレベルB)
- Backwash ileitisの存在は大腸癌発生のリスクとなる。(エビデンスレベルC)
CD関連消化管腫瘍
- 小腸大腸型,大腸型CDは大腸癌のリスクとなる。(エビデンスレベルB)
- CDは小腸癌のリスクとなる。(エビデンスレベルB)
- 肛門病変を有するCD患者は直腸肛門管癌のリスクとなる。(エビデンスレベルC)
● 解説
UC関連大腸腫瘍
2001年のEadenらの報告によればUCにおける大腸癌発生のリスクは診断10年後付近から上昇し,10年で2%,20年で8%,30年で18%と推定されている1)。一方,European Crohn’s and Colitis Organization(ECCO)ガイドライン20172)においては近年のpopulation-based studyでは発症リスクは以前と比較して下がっていると述べられている。例えばニュージーランドのコホート研究では518人のUC患者が追跡され,総発生率は1.35/1,000人年(95%信頼区間0.74-2.27),ニュージーランドの人口と比較して年齢調整された標準化罹患率は1.74(95%信頼区間1.03-2.93)であった3)。予後については本邦のMatsuokaらがUC関連大腸癌全体で5年生存率89%,特にStage Ⅱ以下の症例では一般的な大腸癌と差が無いと報告しており,早期発見の増加に伴い改善傾向にある4)。ただ,コホート研究によっては未だに予後は不良とするものもあり,国や地域によって結果は異なっている5,6)。
ECCOガイドライン2)やthe British Society of Gastroenterologyガイドライン7)ではUC関連大腸癌のリスク因子としては長期の罹病期間,内視鏡的・病理組織学的全大腸炎型(直腸炎型では上昇は認めない)8),疾患活動性,炎症性ポリープの存在,大腸癌家族歴,PSC合併例9)が挙げられている。Leuven大学とオランダのコホートを合わせた検討では,UCであること,PSC合併,50%以上のextensive disease,炎症性ポリープの4項目をリスク因子として設定しスコア化を試みている10)。ただし,罹病期間が短くてもUC関連大腸癌の発生が報告されている。Cohen-Mekelburgらは単施設93人のIBD関連大腸癌を解析したところ11人(11.8%)が発症から8年以内であった11)。本邦からもHataらがUC関連大腸癌のうち17%が発症から8年未満で発見されていたと報告している12)。これらの事実から,罹病期間のみを頼るのではなく,個々の患者において他のリスク因子,治療歴や活動性の強度なども考慮に入れてサーベイランス大腸内視鏡検査を考える必要がある。
UCのbackwash ileitisについては大腸癌のリスクになるという報告13)とdysplasiaまでのリスクにとどまるとする報告14)がある。そのメカニズムについては明らかになっていないが,backwash ileitisの存在と同じく発癌リスクと考えられているPSC合併との関連性を示唆する報告がある13)。興味深い報告として,虫垂切除術はUCの発症に防御的に働くことは知られているが,逆に虫垂切除術がUC関連大腸癌発生のリスクになるのではないかという議論が存在する15-17)。
CD関連消化管腫瘍
CD関連消化管腫瘍に関する知見はUC関連大腸腫瘍に比べて限られているが,大腸病変についてはUCと同様に大腸癌発生のリスクとなると考えられておりサーベイランス大腸内視鏡検査の適応である2,7)。
スウェーデンとデンマークのコホート研究では,1969~2017年にCDを発症した47,035人の患者と463,187人の性,年齢等を調整した比較対照群とを比較した。CD患者では296人(1,000人年あたり0.47人)の大腸癌死亡が発生し,比較対照群では1,968人(1,000人年あたり0.31人)であり,全体的な調整後のハザード比(HR)は1.74(95%信頼区間 1.54-1.96)であった。CD患者では比較対照群より大腸癌死亡の率が高かった18)。CanavanらのメタアナリシスではCD全体での大腸癌相対リスクは2.5(95%信頼区間1.3-4.7),大腸型(Colonic disease)では4.5(95%信頼区間1.3-14.9),回腸型(ileal disease)では1.1(95%信頼区間0.8-1.5)であった19)。累積リスク分析では,CDの診断から10年後時点で大腸癌の相対リスクは2.9(95%信頼区間1.5-5.3)であり過去30年間で減少傾向にあった。一方,CDにおける小腸癌の相対リスクは33.2(95%信頼区間15.9-60.9)であり,大腸癌のリスクが減少しているのに対して,小腸癌の相対リスクは,過去30年間で大幅な減少は認めなかった。2004年5月~2005年6月にかけてフランスで行われた観察研究に登録された炎症性腸疾患19,486人の患者の追跡調査が行われた。年齢と性別を一致させた症例対照研究を行ったところ,IBDの8人が肛門管癌を発症し,14人の患者が直腸癌を発症した。コホートエントリー時に肛門・肛門周囲の病変あるいはその既往があった2,911人の患者のサブグループでは,2人が肛門扁平上皮癌を発症し,3人が痔瘻癌を発症し,6人が直腸癌を発症した。発生率は,肛門扁平上皮癌では1,000人年あたり0.26,痔瘻癌では1,000人年あたり0.38,直腸癌では1,000人年あたり0.77であった。一方,肛門病変を伴わないUCまたはCDの16,575人の患者のうち,肛門管癌の発生率は1,000患者年あたり0.08であり,直腸癌の発生率は1,000患者年あたり0.21であった。単変量解析では,コホートエントリー時の過去または現在の肛門病変の存在が肛門管癌の発症に有意に関連する唯一の要因として抽出された(オッズ比11.2,95%信頼区間1.18-551.51,p=0.03)20)。この結果からは肛門部病変を有するCD患者では有しないCD患者あるいはUC患者と比較して,肛門管癌や直腸癌発生のリスクが高いと考えられる。
文献
- Eaden JA, Abrams KR, Mayberry JF:The risk of colorectal cancer in ulcerative colitis:a meta-analysis. Gut 2001;48:526-535.
- van Rheenen PF, Aloi M, Biron IA, et al.:European Crohn’s and Colitis Organisation Topical Review on Transitional Care in Inflammatory Bowel Disease. J Crohns Colitis 2017;11:1032-1038
- Tranter-Entwistle I, Mullaney TG, Noah K, et al.:Long-term incidence of dysplasia and colorectal cancer in an ulcerative colitis population-based cohort. ANZ J Surg 2020;90:821-825
- Matsuoka H, Ikeuchi H, Uchino M, et al.:Clinicopathological features of ulcerative colitis-associated colorectal cancer pointing to efficiency of surveillance colonoscopy in a large retrospective Japanese cohort. Int J Colorectal Dis 2013;28:829-834
- Bogach J, Pond G, Eskicioglu C, et al.:Age-Related Survival Differences in Patients With Inflammatory Bowel Disease-Associated Colorectal Cancer:A Population-Based Cohort Study. Inflamm Bowel Dis 2019;25:1957-1965
- Kunovszki P, Milassin Á, Gimesi-Országh J, et al.:Epidemiology, mortality and prevalence of colorectal cancer in ulcerative colitis patients between 2010-2016 in Hungary―a population-based study. PLoS One 2020;15:e0233238
- Lamb CA, Kennedy NA, Raine T, et al.;IBD guidelines eDelphi consensus group:British Society of Gastroenterology consensus guidelines on the management of inflammatory bowel disease in adults. Gut 2019;68(Suppl 3):s1-s106
- Beaugerie L, Svrcek M, Seksik P, et al.;CESAME Study Group:Risk of colorectal high-grade dysplasia and cancer in a prospective observational cohort of patients with inflammatory bowel disease. Gastroenterology 2013;145:166-175
- Torres J, Pineton de Chambrun G, Itzkowitz S, et al.:Review article:colorectal neoplasia in patients with primary sclerosing cholangitis and inflammatory bowel disease. Aliment Pharmacol Ther 2011;34:497-508
- Lutgens M, Vermeire S, Van Oijen M, et al.:Dutch Initiative on Crohn and Colitis. A rule for determining risk of colorectal cancer in patients with inflammatory bowel disease. Clin Gastroenterol Hepatol 2015;13:148-154.e1
- Cohen-Mekelburg S, Schneider Y, Gold S, et al.:Risk of Early Colorectal Cancers Needs to Be Considered in Inflammatory Bowel Disease Care. Dig Dis Sci 2019;64:2273-2279
- Hata K, Anzai H, Ikeuchi H, et al.;Research Group for Intractable Inflammatory Bowel Disease of the Ministry of Health, Labour and Welfare of Japan(RGIBD):Surveillance Colonoscopy for Ulcerative Colitis-Associated Colorectal Cancer Offers Better Overall Survival in Real-World Surgically Resected Cases. Am J Gastroenterol 2019;114:483-489
- Heuschen UA, Hinz U, Allemeyer EH, et al.:Backwash ileitis is strongly associated with colorectal carcinoma in ulcerative colitis. Gastroenterology 2001;120:841-847
- Navaneethan U, Jegadeesan R, Gutierrez NG, et al.:Backwash ileitis and the risk of colon neoplasia in ulcerative colitis patients undergoing restorative proctocolectomy. Dig Dis Sci 2013;58:2019-2027
- Stellingwerf ME, Bemelman WA, Löwenberg M, et al.;Parelsnoer Institute, the Dutch Initiative on Crohn, Colitis:A nationwide database study on colectomy and colorectal cancer in ulcerative colitis:what is the role of appendectomy? Colorectal Dis 2021;23:64-73
- Stellingwerf ME, de Koning MA, Pinkney T, et al.:The Risk of Colectomy and Colorectal Cancer After Appendectomy in Patients With Ulcerative Colitis:A Systematic Review and Meta-analysis. J Crohns Colitis 2019;13:309-318
- Gordillo J, Cabré E, Garcia-Planella E, et al.;ENEIDA Project of the Spanish Working Group in Crohn’s Disease and Ulcerative Colitis(GETECCU):Thiopurine Therapy Reduces the Incidence of Colorectal Neoplasia in Patients with Ulcerative Colitis. Data from the ENEIDA Registry. J Crohns Colitis 2015;9:1063-1070
- Olén O, Erichsen R, Sachs MC, et al.:Colorectal cancer in Crohn’s disease:a Scandinavian population-based cohort study. Lancet Gastroenterol Hepatol 2020;5:475-484
- Canavan C, Abrams KR, Mayberry J. Meta-analysis:colorectal and small bowel cancer risk in patients with Crohn’s disease. Aliment Pharmacol Ther 2006;23:1097-1104
- Beaugerie L, Carrat F, Nahon S, et al.;Cancers et Surrisque Associé aux Maladies Inflammatoires Intestinales En France Study Group:High Risk of Anal and Rectal Cancer in Patients With Anal and/or Perianal Crohn’s Disease. Clin Gastroenterol Hepatol. 2018;16:892-899.e2
CQ 3:IBD関連消化管腫瘍の臨床病理学的特徴は,日本人と欧米人との間に違いはあるか?
UC関連大腸腫瘍
日本人と欧米人との間にUC関連大腸腫瘍の臨床病理学的特徴に差はないと推測される。(エビデンスレベルD)
CD関連消化管腫瘍
CD関連消化管腫瘍には,発癌部位や組織型に地域あるいは人種差が見られる。アジアでは直腸肛門管癌が大部分を占め,粘液癌が多いのが特徴である。(エビデンスレベルC)
● 解説
IBD関連消化管腫瘍に対する地域あるいは人種による差に関する報告は多くない。しかし癌化リスクの報告や遺伝子変異の報告は時に異なることがあり,何らかの差異が存在する可能性はある。以下に疾患ごとに分けて解説を述べる。
UC関連大腸腫瘍
UC関連大腸癌では粘液癌や印環細胞癌の頻度が散発性大腸癌よりも高い可能性が報告されているが,欧米と本邦での組織学的な差については報告されていない1)。またp53,APC,KRASなどの遺伝子変異もUC関連大腸癌と散発性大腸癌でその発現に差があることは報告されているが,やはり地域あるいは人種による差は報告されていない2-4)。
欧米の報告ではPSCの合併が発癌リスクに挙げられているが,本邦ではPSC自体の頻度が低く,癌化のメカニズムに相違がある可能性はあるものの明確ではない5-7)。UCに対するサーベイランス大腸内視鏡検査の推奨は本邦と欧米に大きな差異はなく,いずれも左側大腸の癌/dysplasiaが多いという共通点から予測すると,UC関連大腸癌は臨床病理学的には欧米と類似していると考えられる5-8)。
CD関連消化管腫瘍
CD関連消化管腫瘍に関しては,これまで報告された症例報告,ケースシリーズ,コホート研究をもとに2021年にシステマティックレビューおよびメタアナリシスが行われている9)。CD関連消化管腫瘍では小腸癌,大腸癌ともに標準化罹患率は高いとされているが,有病率は大腸癌57/7,344(0.77%),小腸癌17/7,344(0.23%)であり,リスクは高くなるものの特に小腸癌での有病率は高くないことが示されている。
大腸癌の病変に関しては地域差または人種差がある可能性がある。欧米の3コホート研究(合計103大腸癌症例)を見ると右側結腸癌36.9%,左側大腸癌63.1%で左側大腸癌の頻度は高いものの,散発性大腸癌と比べると右側結腸癌の頻度が高くなっている。アジアからの17報告,合計107症例の内容では右側結腸癌15.9%,左側大腸癌84.1%と左側大腸癌,特に直腸肛門管癌が大部分を占めていた。
CD関連直腸肛門管癌は54論文,208症例が報告されていた。人種や地域に関する記載は少なく詳細な検討は不可能であったが,組織型は扁平上皮癌49例,腺癌125例(粘液癌も含む),その他34例であり,扁平上皮癌は48/49(98%)が欧米の報告であった。アジアの報告64例での扁平上皮癌は1例のみで,残りの大部分が粘液癌を含む腺癌であった。
以上のように発癌部位,組織型には地域あるいは人種差が存在する可能性があるが,報告例におけるその情報は少ない。また,英文報告例のみのレビューであり,すべての症例を把握できていないため,明らかなエビデンスをもってその違いには言及できない。
文献
- Watanabe T, Konishi T, Kishimoto J, et al.;Japanese Society for Cancer of the Colon and Rectum:Ulcerative colitis-associated colorectal cancer shows a poorer survival than sporadic colorectal cancer:a nationwide Japanese study. Inflamm Bowel Dis 2011;17:802-808
- Burmer GC, Rabinovitch PS, Haggitt RC, et al.:Neoplastic progression in ulcerative colitis:histology, DNA content, and loss of a p53 allele. Gastroenterology 1992;103:1602-1610
- Robles AI, Traverso G, Zhang M, et al.:Whole-Exome Sequencing Analyses of Inflammatory Bowel Disease-Associated Colorectal Cancers. Gastroenterology 2016;150:931-943
- Klampfer L:Cytokines, inflammation and colon cancer. Curr Cancer Drug Targets 2011;11:451-464
- Rubin DT, Ananthakrishnan AN, Siegel CA, et al.:ACG Clinical Guideline:Ulcerative Colitis in Adults. Am J Gastroenterol 2019;114:384-413
- Magro F, Gionchetti P, Eliakim R, et al.;European Crohn’s and Colitis Organisation[ECCO]:Third European Evidence-based Consensus on Diagnosis and Management of Ulcerative Colitis. Part 1:Definitions, Diagnosis, Extra-intestinal Manifestations, Pregnancy, Cancer Surveillance, Surgery, and Ileo-anal Pouch Disorders. J Crohns Colitis 2017;11:649-670
- Annese V, Beaugerie L, Egan L, et al.;ECCO:European Evidence-based Consensus:Inflammatory Bowel Disease and Malignancies. J Crohns Colitis. 2015;9:945-965
- 日本消化器病学会編:炎症性腸疾患(IBD)診療ガイドライン2020(改訂第2版)https://www.jsge.or.jp/committees/guideline/guideline/pdf/ibd2020_.pdf(15 December 2021 accessed)
- Uchino M, Ikeuchi H, Hata K, et al.:Intestinal cancer in patients with Crohn’s disease:A systematic review and meta-analysis. J Gastroenterol Hepatol 2021;36:329-336
CQ 4:IBDに対する薬物療法は関連消化管腫瘍発生リスクに影響するか?
- 1.2 g/日以上の5-ASA製剤内服はUC関連大腸癌リスクを下げる。(エビデンスレベルB)
- チオプリン製剤の投与は,IBD,特にUC関連大腸腫瘍発生リスクを下げる可能性がある。(エビデンスレベルC)
● 解説
IBD関連消化管腫瘍発生のリスクとなる薬物療法を示した報告は認めなかった。リンパ腫や非黒色腫性皮膚癌のリスク因子として知られるチオプリン製剤においても,関連消化管腫瘍発生リスクを増やす報告は認めなかった。そのため,本CQにおいてはIBD治療薬の関連消化管腫瘍発生に対する予防効果について記述する。
5-アミノサリチル酸(5-aminosalicylic acid:5-ASA)製剤
5-ASA製剤の内服がUC関連大腸癌の発生に予防的に作用するという報告は数多くある。LyakhovichとGascheらのシステマティックレビューでは,発癌の化学的予防メカニズムについては細胞周期進行への干渉,活性酸素または窒素由来代謝物の除去,サイトカインシグナル伝達への干渉伝達,WNT/ベータカテニンシグナルへの関与などが報告されている1)。O’Connorらのメタアナリシスでは5-ASA製剤1.2 g/日以上が大腸腫瘍発生リスクを下げることが報告されている(OR 0.5,95%信頼区間0.3-0.9,p=0.02)。なおスルファサラジンにはこの作用は認められなかった2)。Qiuらにメタアナリシスでは1.2 g/日以上の5-ASA製剤が炎症性腸疾患の大腸癌発生率を下げることが示されたが,dysplasiaの発生率を抑制することはなかった。化学予防の作用はCDよりもUCで顕著であった3)。Bonovasらのメタアナリシスでもスルファサラジンよりも5-ASA製剤で用量依存性に大腸癌やdysplasiaに対する予防効果が高く,CDよりもUCでその効果は高かった4)。その他にもUC関連大腸癌に5-ASA製剤の化学予防効果に関するメタアナリシスの結果が示されている5-7)。しかしながら,生物学的製剤と5-ASA製剤の併用により寛解状態にある患者において5-ASA製剤を休薬することについて,大腸癌予防の点から検討したデータは乏しい。
スルファサラジン
スルファサラジンにおいては,複数のメタアナリシスによるとIBD関連消化管腫瘍発生の予防に関与しないとされており2,3),UC・CDともに関連消化管腫瘍発生の予防目的での投与は強く推奨しない。
チオプリン製剤
チオプリン製剤では,IBD関連消化管腫瘍発生の予防効果を検討した4件のメタアナリシスがあり8-11),そのうち3件において,UC関連大腸腫瘍発生の予防効果が示されている8-10)。一方で,広範な大腸炎やPSC合併例では予防効果を認めなかった8),研究の不均一性がある10),と報告されている。UCとCDにおける予防効果の違いを分けて検討した報告は1件のみ9)であり,UC(OR 0.67,95%信頼区間0.45-0.98,p=0.006)に比してCD(OR 1.06,95%信頼区間0.54-2.09,p=0.535)では有意な予防効果を認めなかった。IBD患者全体を検討した報告が目立つ中,UC単独での予防効果を支持する報告はあるが,CD単独では予防効果を支持しないと報告されている。すべてのメタアナリシスに含まれる文献にランダム化比較試験がないことからエビデンスレベルCとした。
ウルソデオキシコール酸(UDCA)
UDCAは,PSCの治療薬として使用される機会が多い。PSCを合併したIBDでは関連消化管癌のリスクが高いことが知られている。プラセボ対照ランダム化比較試験にて,UDCAを投与したPSC合併UC患者において関連大腸癌発生の予防効果が報告された12)一方で,高用量UDCA(28~30 mg/kg/日)投与群においてプラセボより有意にUC関連大腸腫瘍が増加するという報告がある13)。その後のメタアナリシスでは,UDCA投与と関連大腸腫瘍発生の関連性は示されなかった(リスク比0.87,95%信頼区間0.51-1.49,p=0.62)14)。低用量UDCAでのエビデンスも不足しており,関連消化管腫瘍発生の予防目的でのUDCA投与は推奨されない。
生物学的製剤
抗TNFα抗体製剤が関連消化管腫瘍発生を予防したとする報告は認められなかった15-17)。新規治療薬が増えてきていることから今後のエビデンス集積が望まれる。
その他薬剤
アスピリンが,遺伝素因やIBDに関連しない散発性大腸癌発生の予防に関与するという報告がある18)。Non-steroidal anti-inflammatory drugs(NSAIDs)・アスピリンにおけるIBD関連消化管癌の予防に関するメタアナリシス19)では,研究間の異質性が高く(I2>50%),質の高いエビデンスが不足している。利用可能なエビデンスからは,これら薬剤における関連消化管腫瘍発生の有意な予防効果は認めなかった。
スタチンや葉酸の関連消化管腫瘍発生の予防効果を検討した研究によると,スタチンは関連消化管腫瘍発生リスクの減少に関与していなかった(リスク比0.98,95%信頼区間0.43-2.25,p=0.96)20)。葉酸に関しては,後ろ向きコホート研究の1報告のみであり現時点ではエビデンス不足である21)。
以上のように,5-ASAおよびチオプリン製剤の投与には,IBD,特にUC関連消化管腫瘍発生抑制効果が示されているが,これが薬剤自体の効果かIBDの重症度の軽減によるものかに関しては未だ不明である。
文献
- Lyakhovich A, Gasche C:Systematic review:molecular chemoprevention of colorectal malignancy by mesalazine. Aliment Pharmacol Ther 2010;31:202-209
- O’Connor A, Packey CD, Akbari M, et al.:Mesalamine, but not sulfasalazine, reduces the risk of colorectal neoplasia in patients with inflammatory bowel disease. Inflamm Bowel Dis 2015;21:2562-2569
- Qiu X, Ma J, Wang K, et al.:Chemopreventive effects of 5-aminosalicylic acid on inflammatory bowel disease-associated colorectal cancer and dysplasia:a systematic review with meta-analysis. Oncotarget 2017;8:1031-1045
- Bonovas S, Fiorino G, Lytras T, et al.:Systematic review with meta-analysis:use of 5-aminosalicylates and risk of colorectal neoplasia in patients with inflammatory bowel disease. Aliment Pharmacol Ther 2017;45:1179-1192
- Zhao LN, Li JY, Yu T, et al.:5-Aminosalicylates Reduce the Risk of Colorectal Neoplasia in Patients with Ulcerative Colitis:An Updated Meta-Analysis. PLoS One 2014;9:e94208
- Velayos FS, Terdiman JP, Walsh JM:Effect of 5-aminosalicylate use on colorectal cancer and dysplasia risk:a systematic review and metaanalysis of observational studies. Am J Gastroenterol 2005;100:1345-1353
- Akobeng AK, Gardener E:Oral 5-aminosalicylic acid for maintenance of medically-induced remission in Crohn’s disease. Cochrane Database Syst Rev 2016;9:CD003715
- Zhu Z, Mei Z, Guo Y, et al.:Reduced risk of inflammatory bowel disease-associated colorectal neoplasia with use of thiopurines:a systematic review and meta-analysis. J Crohns Colitis 2018;12:546-558
- Lu MJ, Qiu XY, Mao XQ, et al.:Systematic review with meta-analysis:thiopurines decrease the risk of colorectal neoplasia in patients with inflammatory bowel disease. Aliment Pharmacol Ther 2018;47:318-331
- Gong J, Zhu L, Guo Z, et al.:Use of Thiopurines and Risk of Colorectal Neoplasia in Patients with Inflammatory Bowel Diseases:A Meta-Analysis. PLoS One 2013;8:e81487
- Jess T, Lopez A, Anderson M, et al.:Thiopurines and risk of colorectal neoplasia in patients with inflammatory bowel disease:a meta-analysis. Clin Gastroenterol Hepatol 2014;12:1793-1800
- Pardi DS, Loftus EV Jr, Kremers WK, et al.:Ursodeoxycholic acid as a chemopreventive agent in patients with ulcerative colitis and primary sclerosing cholangitis. Gastroenterology 2003;124:889-893
- Eaton JE, Silveira MG, Pardi DS, et al.:High-dose ursodeoxycholic acid is associated with the development of colorectal neoplasia in patients with ulcerative colitis and primary sclerosing cholangitis. Am J Gastroenterol 2011;106:1638-1645
- Hansen JD, Kumar S, Lo WK, et al.:Ursodiol and Colorectal Cancer or Dysplasia Risk in Primary Sclerosing cholangitis and Inflammatory Bowel Disease:A Meta-Analysis. Dig Dis Sci 2013;58:3079-3087
- Charkaoui M, Hajage D, Tubach F, et al.:Impact of Anti-tumour Necrosis Factor Agents on the Risk of Colorectal Cancer in Patients with Ulcerative Colitis:Nationwide French Cohort Study. J Crohns Colitis 2022;16:893-899
- Alkhayyat M, Abureesh M, Gill A, et al.:Lower Rates of Colorectal Cancer in Patients With Inflammatory Bowel Disease Using Anti-TNF Therapy. Inflamm Bowel Dis 2021;27:1052-1060
- Baars JE, Looman CWN, Steyerberg EW, et al.:The risk of inflammatory bowel disease-related colorectal carcinoma is limited:results from a nationwide nested case-control study. Am J Gastroenterol 2011;106:319-328
- Rothwell PM, Wilson M, Elwin CE, et al.:Long-term effect of aspirin on colorectal cancer incidence and mortality:20-year follow-up of five randomised trials. Lancet 2010;376:1741-1750
- Burr NE, Hull MA, Subramanian V:Does aspirin or non-aspirin non-steroidal anti-inflammatory drug use prevent colorectal cancer in inflammatory bowel disease? World J Gastroenterol 2016;22:3679-3686
- Shah SC, Glass J, Giustino G, et al.:Statin Exposure Is Not Associated with Reduced Prevalence of Colorectal Neoplasia in Patients with Inflammatory Bowel Disease. Gut Liver 2019;13:54-61
- Burr NE, Hull MA, Subramanian V, et al.:Folic Acid Supplementation May Reduce Colorectal Cancer Risk in Patients With Inflammatory Bowel Disease:A Systematic Review and Meta-Analysis. J Clin Gastroenterol 2017;51:247-253
CQ 5:IBD関連消化管腫瘍に対する内視鏡によるサーベイランスは有効か?
サーベイランス大腸内視鏡検査は,IBD関連消化管腫瘍,特に癌を早期に発見することで予後を改善する可能性があり,行うことを強く推奨する。(推奨度1・エビデンスレベルC,合意率:86%)
● 解説
IBD症例ではサーベイランス大腸内視鏡検査の重要性が提唱されている。サーベイランス大腸内視鏡検査により大腸癌発症や死亡リスクを低減することに関するランダム化比較試験はないが,複数のコホート研究や症例対照研究ではサーベイランス大腸内視鏡群により早期に大腸癌を発見することができ,大腸癌関連の良好な予後への寄与や費用対効果が高いことが示されている1-12)。
Lutgensらは,後ろ向きコホート研究によるIBD患者における大腸癌診断時のTNM分類におけるStage 0およびⅠの割合が,サーベイランス大腸内視鏡群では52%,非サーベイランス群では24%(p=0.004)であること,また大腸癌診断後の5年生存率が,サーベイランス大腸内視鏡群では100%であったのに対し,非サーベイランス群では74%であり(p=0.042),サーベイランス大腸内視鏡群ではより多くの腫瘍が早期に発見され大腸癌による死亡もサーベイランス大腸内視鏡群で有意に少ないことを報告している2)。
コクラン・レビューでは,内視鏡的サーベイランスはIBDにおける大腸癌やdysplasiaを早期に発見することで延命効果の可能性があると報告されている13)。プール解析では,内視鏡的サーベイランス群は非サーベイランス群と比較し,早期の大腸癌発見が多く(16% vs. 8%,OR 5.40,95%信頼区間1.51-19.30,p=0.009),死亡率も低い(8% vs. 22%,OR 0.36,95%信頼区間0.19-0.69,p=0.002)と報告されている13)。
以上,エビデンスレベルは低いものの,IBD関連消化管腫瘍に対するサーベイランス大腸内視鏡検査は大腸癌関連予後の改善を期待できる。
文献
- Löfberg R, Broström O, Karlén P, et al.:Colonoscopic surveillance in long standing total ulcerative colitis―a 15-year follow-up study. Gastroenterology 1990;99:1021-1031
- Lutgens MW, Oldenburg B, Siersema PD, et al.:Colonoscopic surveillance improves survival after colorectal cancer diagnosis in inflammatory bowel disease. Br J Cancer 2009;101:1671-1675
- Eaden J, Abrams K, Ekbom A, et al.:Colorectal cancer prevention in ulcerative colitis:a case-control study. Aliment Pharmacol Ther 2000;14:145-153
- Ananthakrishnan AN, Cagan A, Cai T, et al.:Colonoscopy is associated with a reduced risk for colon cancer and mortality in patients with inflammatory bowel diseases. Clin Gastroenterol Hepatol 2015;13:322.e1-329.e1
- Farraye FA, Odze RD, Eaden J, et al.:AGA technical review on the diagnosis and management of colorectal neoplasia in inflammatory bowel disease. Gastroenterology 2010;138:746-774. 774 e1-4;quiz e12-13
- Itzkowitz SH, Present DH;Crohn’s and Colitis Foundation of America Colon Cancer in IBD Study Group:Consensus conference:colorectal cancer screening and surveillance in inflammatory bowel disease. Inflamm Bowel Dis 2005;11:314-321
- American Society for Gastrointestinal Endoscopy Standards of Practice Committee;Shergill AK, Lightdale JR, Bruining DH, et al.:The role of endoscopy in inflammatory bowel disease. Gastrointest Endosc 2015;81:1101-1121. e1-13
- Magro F, Gionchetti P, Eliakim R, et al.:Third European Evidence-based Consensus on Diagnosis and Management of Ulcerative Colitis. Part 1:Definitions, Diagnosis, Extra-intestinal Manifestations, Pregnancy, Cancer Surveillance, Surgery, and Ileo-anal Pouch Disorders. J Crohns Colitis 2017;11:649-670
- Kornbluth A, Sachar DB;Practice Parameters Committee of the American College of Gastroenterology. Ulcerative colitis practice guidelines in adults:American College of Gastroenterology, Practice Parameters Committee. Am J Gastroenterol 2010;105:501-523;quiz 524
- Cairns SR, Scholefield JH, Steele RJ, et al.:Guidelines for colorectal cancer screening and surveillance in moderate and high risk groups(update from 2002). Gut 2010;59:666-689
- Annese V, Daperno M, Rutter MD, et al.:European evidence based consensus for endoscopy in inflammatory bowel disease. J Crohns Colitis 2013;7:982-1018
- Laine L, Kaltenbach T, Barkun A, et al.:SCENIC international consensus statement on surveillance and management of dysplasia in inflammatory bowel disease. Gastroenterology 2015;148:639-651. e28
- Bye WA, Nguyen TM, Parker CE, et al.:Strategies for detecting colon cancer in patients with inflammatory bowel disease. Cochrane Database Syst Rev 2017;9:CD000279
CQ 6:サーベイランスにおける最適な内視鏡検査の方法(開始時期,施行間隔,観察方法など)は何か?
- UCでは発症から8年後以降は大腸内視鏡検査を行うことを推奨する。ただし,PSCを伴う患者に対しては,診断時にサーベイランスを開始することを推奨する。(推奨度2・エビデンスレベルC,合意率:71%)
- 左側大腸炎型,大腸の1/3以上に病変を有する,あるいは全大腸炎型UC患者では,1~2年に一度のサーベイランス大腸内視鏡検査を行うことを推奨する。ただし,PSCを伴う患者に対しては毎年のサーベイランスが推奨される。(推奨度2・エビデンスレベルC,合意率:93%)
- UCにおけるサーベイランス大腸内視鏡検査ではインジゴカルミンなどの色素内視鏡検査が推奨される。(推奨度2・エビデンスレベルB,合意率:推奨度1;52%,推奨度2;48%)
● 解説
どの時点からサーベイランスを開始すべきかについての明らかなランダム化比較試験またはシステマティックレビューは認められないが,複数の文献において,8年以上罹病期間のあるIBD患者においてサーベイランス大腸内視鏡検査を行った結果が複数報告されており1,2),少なくとも8年の罹患期間がある場合必ず大腸内視鏡検査によるサーベイランスを施行することが望ましいと考えられる。しかしながら8年未満でのUC関連大腸癌の発生も報告されているため注意が必要である。炎症が存在する場合腫瘍の検出は内視鏡的にも病理学的にも検出が困難になる場合があり,サーベイランスは寛解期に施行することが望ましい。一方で,慢性持続型UCの場合は大腸癌の発生リスクが高い可能性も念頭に置いて内視鏡検査の実施にあたる。
UC患者におけるPSCは大腸癌発生のリスクとされており,診断時からのサーベイランス開始が推奨される3,4)。しかしながらPSCの合併は本邦では比較的まれと考えられている。また本邦ではPSC合併UCにおける大腸癌の発生リスクが欧米と同等であるかどうかは明らかではなく,海外において推奨されているPSC合併症例に対する毎年のサーベイランスを直ちに本邦に外挿できるかどうかは議論のあるところである。
サーベイランスの施行間隔における検討は1~3年と幅がある2,3,5)。近年報告された77,824人のIBD患者における後ろ向きコホート研究では,サーベイランスなしと比較して,1年以内または1~3年以内の大腸内視鏡検査により大腸癌のStageが進行した状態での診断リスクを減少している可能性が示唆された(各々調整OR 0.40(95%信頼区間0.20-0.82),0.56(95%信頼区間0.32-0.98)6)。いずれにせよPSCを伴う患者は発癌リスクが高いため,毎年の検査が推奨される3)。サーベイランスの間隔は,リスクの異なるグループに対しては変更することを推奨する報告もある。遠位大腸炎型の場合,一般集団のサーベイランスプログラムに従うことができるとする報告もある7)。
IBD関連消化管腫瘍に対するサーベイランス大腸内視鏡検査は高解像度の内視鏡システムを用い,色素散布を併用することで大腸癌の罹患率と死亡率を軽減するとする報告があり3),色素散布による狙撃生検によって白色光と比較しnon-polypoid type dysplasiaの検出率が有意に増加したという報告もある8)。腫瘍の既往,PSCの併発,腺腫を認めた場合には色素散布を併用したランダム生検も検討する9)。近年の色素内視鏡検査とnarrow band imaging (NBI)を比較した報告では両者におけるdysplasiaの発見率は差が無かった10,11)。NBIでは検査時間が短く容易に行えることから,今後NBIがサーベイランスに用いられる可能性が示唆されている10)。
文献
- Choi PM, Nugent FW, Schoetz DJ Jr, et al.:Colonoscopic surveillance reduces mortality from colorectal cancer in ulcerative colitis. Gastroenterology 1993;105:418-424
- Lashner BA, Kane SV, Hanauer SB:Colon cancer surveillance in chronic ulcerative colitis:historical cohort study. Am J Gastroenterol 1990;85:1083-1087
- Rabbenou W, Ullman TA:Risk of Colon Cancer and Recommended Surveillance Strategies in Patients with Ulcerative Colitis. Gastroenterol Clin North Am 2020;49:791-807
- Lindberg BU, Broomé U, Persson B:Proximal colorectal dysplasia or cancer in ulcerative colitis. The impact of primary sclerosing cholangitis and sulfasalazine:results from a 20-year surveillance study. Dis Colon Rectum 2001;44:77-85
- Sengupta N, Yee E, Feuerstein JD:Colorectal Cancer Screening in Inflammatory Bowel Disease. Dig Dis Sci 2016;61:980-989.
- Kim HS, Hernaez R, Sansgiry S, et al.:Comparative Effectiveness of Surveillance Colonoscopy Intervals on Colorectal Cancer Outcomes in a National Cohort of Patients with Inflammatory Bowel Disease. Clin Gastroenterol Hepatol 2022;20:2848-2857.e2
- Stolwijk JA, Langers AM, Hardwick JC, et al.:A thirty-year follow-up surveillance study for neoplasia of a dutch ulcerative colitis cohort. Sci World J 2013;2013:274715
- Sekra A, Schauer C, Mills L, et al.:Chromoendoscopy versus standard colonoscopy for detection of nonpolypoid dysplasia in patients with inflammatory bowel disease. N Z Med J 2018;131:32-38
- Moussata D, Allez M, Cazals-Hatem D, et al.:Are random biopsies still useful for the detection of neoplasia in patients with IBD undergoing surveillance colonoscopy with chromoendoscopy? Gut 2018;67:616-624
- Bisschops R, Bessissow T, Joseph JA, et al.:Chromoendoscopy versus narrow band imaging in UC:a prospective randomised controlled trial. Gut 2018;67:1087-1094
- Iannone A, Ruospo M, Wong G, et al.:Chromoendoscopy for Surveillance in Ulcerative Colitis and Crohn’s Disease:A Systematic Review of Randomized Trials. Clin Gastroenterol Hepatol 2017;15:1684-1697.e11
CQ 7:IBD関連消化管腫瘍に対する内視鏡検査以外のサーベイランスは有効か?
現時点では,IBD関連消化管腫瘍に対する内視鏡検査以外の有効なサーベイランス方法は確立されているとはいえない。(推奨度なし・エビデンスレベルC)なお直腸肛門管癌についてはCQ 9を参照。
● 解説
IBD関連消化管腫瘍に対するサーベイランスは大腸内視鏡検査を用いることが推奨され,そのほかの検査方法については明らかなエビデンスがないのが現状である。腫瘍に対する大腸内視鏡検査以外のサーベイランスとして,腫瘍マーカー(CEA,CA19-9),p53等のバイオマーカー,骨盤CT検査やMRI検査が考えられるがその報告はCDにおける直腸病変についてのケースシリーズにとどまるのみである1,2)。CDにおけるpositron emission tomography(PET)検査を用いたサーベイランスに関する遡及的な検討も報告されているが,その有用性は否定的である3)。また,CT等の検査においては放射線被曝によるリスクや,患者本人の金銭的な負担を生じていることにも留意し,コストベネフィットのバランスを考慮して検査を考慮する必要性が考えられる。
そのほかリスク層別化として,便中のDNAからの変異を同定する方法4,5)や,便中カルプロテクチンによるリスク層別化6)の報告が散見される。リーフレットやビデオにより患者への情報提供が有用とする報告もあるが7),いずれも探索的な研究段階であると考えられる。
文献
- 杉田 昭:潰瘍性大腸炎,Crohn病に合併した小腸,大腸癌の特徴と予後―第15報――Crohn病の直腸肛門管癌(痔瘻癌を含む)に対するsurveillance programの検証―.令和1年度厚生労働科学研究補助金(難治性疾患政策研究事業)難治性炎症性腸管障害に関する調査研究 分担研究報告書(令和元年度),2020
- Yoshizawa S, Matsuoka K, Inoue N, et al.:Clinical significance of serum p53 antibodies in patients with ulcerative colitis and its carcinogenesis. Inflamm Bowel Dis 2007;13:865-873.
- Hirano Y, Futami K, Higashi D, et al.:Anorectal cancer surveillance in Crohn’s disease. J Anus Rectum Colon 2018;2:145-154
- Viennot S, Deleporte A, Moussata D, et al.:Colon cancer in inflammatory bowel disease:recent trends, questions and answers. Gastroenterol Clin Biol 2009;33 Suppl 3:S190-S201
- Johnson DH, Taylor WR, Aboelsoud MM, et al.:DNA Methylation and Mutation of Small Colonic Neoplasms in Ulcerative Colitis and Crohn’s Colitis:Implications for Surveillance. Inflamm Bowel Dis 2016;22:1559-1567
- Mooiweer E, Fidder HH, Siersema PD, et al.:Fecal calprotectin testing can identify ineffective colorectal cancer surveillance procedures in patients with longstanding colitis. Inflamm Bowel Dis 2014;20:1079-1084
- Eaden J, Abrams K, Shears J, et al.:Randomized controlled trial comparing the efficacy of a video and information leaflet versus information leaflet al.one on patient knowledge about surveillance and cancer risk in ulcerative colitis. Inflamm Bowel Dis 2002;8:407-412
CQ 8:大腸内視鏡検査によるサーベイランスにおける最適な生検方法は何か?
- UC関連大腸腫瘍に対するサーベイランス大腸内視鏡検査では,色素内視鏡観察等を用いた詳細な内視鏡観察による狙撃生検が推奨される。(推奨度2・エビデンスレベルB,合意率:推奨度1;59%,推奨度2;37%)
- UC関連大腸腫瘍に対するサーベイランス大腸内視鏡検査では,患者の病歴や内視鏡所見,内視鏡医の技量などを参考に,ランダム生検の施行と方法を検討する。(推奨度なし・エビデンスレベルB)
- CDにおけるサーベイランス大腸内視鏡検査の意義や方法は未確立なため,その生検方法も未確立である。(推奨度なし・エビデンスレベルC)
● 解説
本邦で行われた白色光観察を主体としたランダム化比較非劣性試験により,UCサーベイランス大腸内視鏡検査において,狙撃生検はランダム生検と同等の腫瘍性病変発見率であることが示された1)。この研究は,罹病期間7年以上の全大腸炎型および左側大腸炎型UC患者を対象に高画素内視鏡による白色光観察を用い,狙撃生検群は腫瘍性病変が疑わしい所見に対する狙撃生検に直腸下部のランダム生検での1個検体採取を加えて行われ,ランダム生検群は10 cmごとに4個のランダム生検施行に内視鏡医により腫瘍性病変が疑わしいと判断された所見に対する狙撃生検を加える,という方法で行われた。色素内視鏡(拡大)観察は内視鏡医が必要かつ施行可能と判断された場合に併用された。一方,ランダム生検でなければ検出が困難と思われる内視鏡検査で視認困難なdysplasiaが存在する2-4)。UCとCDの連続した1,000例におけるインジゴカルミン溶液によるpanchromoendoscopyを用いた観察研究では,ランダム生検によりdysplasiaの検出率が15%増加したことが示されている3)。この研究では,可視的な腫瘍を疑う病変周辺背景粘膜のランダム生検も行われているが,鉛管様外観,PSC,過去のdysplasiaを有する患者にはランダム生検が有効であると述べている。しかしながら,ランダム生検は10 cmごとに4つのサンプルを採取する方法が世界のガイドライン等ではスタンダードとされており5),内視鏡検査に要する時間の長さや病理医の多数の検体を病理診断する負担の観点から,臨床の場では現実的でない。直腸とS状結腸がUC関連大腸腫瘍の発生頻度が高い領域であるため2),色調や粘膜表面パターンの変化などを手掛かりとした疑わしい病変からの狙撃生検に加えて,これらの領域からのランダム生検を行っている施設も存在する。ランダム生検には,設定したUC炎症進展範囲領域の大腸粘膜をランダムに生検するものと内視鏡で可視的なUC関連大腸腫瘍を疑う病変の周辺背景粘膜をランダムに生検するものがある。後者については既報の検討結果からも施行が推奨されるが,前者については施行の有無や対象となる大腸の範囲,生検個数など定まったものはなく,UC患者の病歴や内視鏡所見,サーベイランス内視鏡検査施行医の技量なども参考に,生検方法が定められているのが現状である。
Hataらは文献1)のランダム化比較試験に登録された8年以上のUC患者のフォローアップデータを用いて,狙撃生検の長期有効性を検討した。その結果,登録時の大腸内視鏡検査所見でdysplasiaが認められないUC患者が大腸癌を発症する確率は低いことが明らかとなり,狙撃生検によるサーベイランス大腸内視鏡検査が推奨された6)。
一方,CD患者の大腸癌発生率は一般集団より有意に高いため,欧州のガイドラインではサーベイランス大腸内視鏡検査が推奨されている7,8)。しかし,本邦のCD患者のCD関連消化管腫瘍は直腸肛門管領域に圧倒的に多いため,適切なサーベイランス大腸内視鏡検査の方法や生検の方法はまだ確立されていない9,10)。
文献
- Watanabe T, Ajioka Y, Mitsuyama K, et al.:Comparison of Targeted vs Random Biopsies for Surveillance of Ulcerative Colitis-Associated Colorectal Cancer. Gastroenterology 2016;151:1122-1130
- Hata K, Anzai H, Ikeuchi H, et al.:Surveillance colonoscopy for ulcerative colitis-associated colorectal cancer offers better overall survival in real-world surgically resected cases. Am J Gastroenterol 2019;114:483-489
- Moussata D, Allez M, Cazals-Hatem D, et al.:Are random biopsies still useful for the detection of neoplasia in patients with IBD undergoing surveillance colonoscopy with chromoendoscopy? Gut 2018;67:616-624
- Watanabe K, Hida N, Ajioka Y, et al.:Photodynamic diagnosis of endoscopically invisible flat dysplasia in patients with ulcerative colitis by visualization using local 5-aminolevulinic acid-induced photosensitization. Gastrointest Endosc 2010;71:1094-1096
- Laine L, Kaltenbach T, Barkun A, et al.:SCENIC international consensus statement on surveillance and management of dysplasia in inflammatory bowel disease. Gastroenterology 2015;148:639-651.e28
- Hata K, Ishihara S, Ajioka Y, et al.:Long-Term Follow-Up of Targeted Biopsy Yield(LOFTY Study)in Ulcerative Colitis Surveillance Colonoscopy. J Clin Med 2020;9:2286
- Torres J, Caprioli F, Katsanos KH, et al.:Predicting Outcomes to Optimize Disease Management in Inflammatory Bowel Diseases. J Crohns Colitis 2016;10:1385-1394
- Bye WA, Nguyen TM, Parker CE, et al.:Strategies for detecting colon cancer in patients with inflammatory bowel disease. Cochrane Database Syst Rev 2017;2017:CD000279
- Hirano Y, Futami K, Higashi D, et al.:Anorectal cancer surveillance in Crohn’s disease. J Anus Rectum Colon. 2018;2:145-154
- Ueda T, Inoue T, Nakamoto T, et al.:Anorectal Cancer in Crohn’s Disease Has a Poor Prognosis Due to its Advanced Stage and Aggressive Histological Features:a Systematic Literature Review of Japanese Patients. J Gastrointest Cancer 2020;51:1-9
CQ 9:CD関連直腸肛門管癌の診断に麻酔下肛門部観察(examination under anesthesia:EUA)は推奨されるか?
CD関連直腸肛門管癌の診断のため,EUAを行うことを弱く推奨する。(推奨度2・エビデンスレベルD,合意率:89%)
● 解説
CD関連大腸癌の発生部位については,本邦では欧米に比べて遠位大腸に多く,特に直腸肛門管癌が全体の80%を占めたと報告されている1-3)。内視鏡検査による癌サーベイランスが確立されているUCでは4-6),早期診断例の増加につながり予後の向上が導かれているが7),CDでは瘻孔や狭窄の病変のため内視鏡検査が容易でなく,CTやMRIなどの画像診断も,癌の進行度の評価には有用であっても早期発見を導くことは難しい。またFDG-PET検査では炎症と癌の集積の鑑別は難しく,頻度の高い粘液癌への集積率の低さからも早期診断としての有用性は示されていない8,9)。腫瘍マーカーについては,CEA上昇を契機に発見できたCDに合併した痔瘻癌の報告例もあるが,高度の進行癌での発見であり,診断の手掛かりにはなるが,早期診断としての有用性は乏しいと言及されている10)。今のところ有効なサーベイランス法はなくCD関連消化管癌の予後は不良である11,12)。EUAはCDの肛門部診察において有用性は報告されており13),関連した直腸肛門管癌の診断や鑑別にも,同様に有用性が考えられる。
EUAは通常,腰椎麻酔,硬膜外麻酔,あるいは全身麻酔で行い,体位は砕石位もしくはjack-knife位で行う。肛門部の診察では肛門縁近傍ばかりでなく,外陰部,殿部,仙骨部まで広汎に観察を行うため,十分に観察が行える体位,視野をとる。肛門縁の診察では,瘻孔部,潰瘍部,skin tagの生検を行う。直腸肛門管癌の診断には,直腸肛門管粘膜のランダム生検,ならびに肛門管内と瘻管の洗浄細胞診などを行う。肛門狭窄による痛みのために,通常内視鏡観察が困難な症例の場合,EUA施行時に大腸内視鏡検査を併用すると,上部直腸までの観察が可能となる。
CD関連直腸肛門管癌の発生リスクとして,長期罹病期間11,14,15)があげられており,10年以上のCD歴を有する患者を対象とした報告では,EUAにより,15.5%に癌を認めたと報告している。癌診断時の平均年齢は,散発性大腸癌の好発年齢に比べ若年で発症していた。CD発症から癌診断までの病悩期間は平均で20年以上であった16)。同報告ではEUAによる生検がサーベイランスの意義を持つかについて検討しており,すでに進行癌とわかる視診での発見例や,癌による症状を有する症例を除いた症例での検討を行い,癌検出率は4.9%であったと報告している16)。癌の進行度は全例がStage Ⅱで,Stage Ⅲ以上の症例はなかったとし,症状がない状態でのEUAによる生検が,より早期の段階での診断に寄与したことを報告している16)。
EUAでは観察が十分に行える体位をとることができ,痛みを取り除いた状態で,経肛門的組織検査を行うことができるため,CD関連直腸肛門管癌の診断に推奨される。
文献
- Choi PM, Zeling MP:Similarity of colorectal cancer in Crohn’s disease and ulcerative colitis:implications for carcinogenesis and prevention. Gut 1994;35:950-954
- Stahl TJ, Schoetz DJ Jr, Roberts PL, et al.:Crohn’s disease and carcinoma:increasing justification for surveillance? Dis Colon Rectum 1992;35:850-856
- Higashi D, Katsuno H, Kimura H, et al.:Current State of and Problems Related to Cancer of the Intestinal Tract Associated with Crohn’s Disease in Japan. Anticancer Res 2016;36:3761-3766
- Van Assche G, Dignass A, Bokemeyer B, et al.;European Crohn’s and Colitis Organisation:Second European evidence-based consensus on the diagnosis and management of ulcerative colitis part 3:special situations. J Crohns Colitis 2013;7:1-33
- Matsumoto T, Iwao Y, Igarashi M, et al.:Endoscopic and Chromoendoscopic atlas featuring dysplastic lesions in surveillance colonoscopy for patients with long-standing ulcerative colitis. Inflamm Bowel Dis 2008;14:259-264
- Farraye FA, Odze RD, Eaden J, et al.;AGA Institute Medical Position Panel on Diagnosis and Management of Colorectal Neoplasia in Inflammatory Bowel Disease:AGA medical position statement on the diagnosis and management of colorectal neoplasia in inflammatory bowel disease. Gastroenterology 2010;138:738-745
- Hata K, Watanabe T, Kazama S, et al.:Earlier surveillance colonoscopy programme improves survival in patients with ulcerative colitis associated colorectal cancer:results of a 23-year surveillance programme in the Japanese population. Br J Cancer 2003;89:1232-1236
- 池内浩基,中埜廣樹,内野 基,他:クローン病に対するPET検査の有用性の検討.日本大腸肛門病会誌2008;61:303-310
- Delbeke D, Martin WH:PET and PET-CT for evaluation of colorectal carcinoma. Semin Nucl Med 2004;3:209-223
- 佐藤 学,小川 仁,柴田 近,他:Infliximab投与後急激な腫瘍マーカー上昇が診断の契機となったCrohn病合併痔瘻癌の1例.日消誌2010;107:885-892
- Yano Y, Matsui T, Uno H, et al.:Risks and clinical features of colorectal cancer complicating Crohn’s disease in Japanese patients. J Gastroenterol Hepatol 2008;23:1683-1688
- Canavan C, Abrams KR, Mayberry J:Meta-analysis:colorectal and small bowel cancer risk in patients with Crohn’s disease. Aliment Pharmacol Ther 2006;23:1097-1104
- Marzo M, Felice C, Pugliese D, et al.:Management of perianal fistulas in Crohn’s disease:an up-to-date review. World J Gastroenterol 2015;21:1394-1403
- Canavan C, Abrams KR, Mayberry J:Meta-analysis:colorectal and small bowel cancer risk in patients with Crohn’s disease. Aliment Pharmacol Ther 2006;23:1097-1104
- Itzkowitz SH, Yio X:Inflammation and cancer Ⅳ. Colorectal cancer in inflammatory bowel disease:the role of inflammation. Am J Physiol Gastrointest Liver Physiol 2004;287:G7-G17
- Hirano Y, Futami K, Higashi D, et al.:Anorectal cancer surveillance in Crohn’s disease. J Anus Rectum Colon 2018;2:145-154
CQ 10:UC関連大腸腫瘍とsporadic colorectal neoplasia(散発性大腸腫瘍)の鑑別となる内視鏡所見は何か?
- UC炎症の進展範囲や背景粘膜所見に加え,病変の形態や表面構造,辺縁,周辺の平坦病変等を総合的に判断して内視鏡的にUC関連大腸腫瘍とsporadic colorectal neoplasia(散発性大腸腫瘍)の鑑別を検討する。(エビデンスレベルC)
- UC関連大腸腫瘍とsporadic colorectal neoplasia(散発性大腸腫瘍)の内視鏡的鑑別は未確立で,内視鏡所見のみならず臨床情報や病理所見も加え,総合的に鑑別に努める。(エビデンスレベルC)
● 解説
UC関連大腸腫瘍とUC非関連のsporadic colorectal neoplasia(散発性大腸腫瘍)とは,その発生過程が異なるだけでなく,治療方針等も異なるため,鑑別診断を要する。従来,UC関連大腸腫瘍に対するサーベイランス大腸内視鏡検査の分野では本邦で開発された工藤・鶴田分類が既報で多く用いられてきた1)。しかし,工藤・鶴田分類もJ-NET分類も,共にsporadicな大腸腫瘍に対して開発された大腸内視鏡所見分類であり2),UC関連大腸腫瘍での検討は乏しい3)。拡大色素内視鏡観察下の絨毛状の表面構造や細長いあるいは不規則な腺管は,非腫瘍の再生粘膜や寛解粘膜でも認めることがあり注意を要する4)。
UC関連大腸腫瘍とsporadic colorectal neoplasia(散発性大腸腫瘍)との内視鏡的鑑別は,背景粘膜を含む種々の内視鏡所見を総合的に判断して診断が試みられている5)。まず,UCの炎症進展範囲外であればsporadicな大腸腫瘍と診断する6)。病変がUC関連大腸腫瘍の好発部位であるS状結腸,直腸以外の部位に存在する場合は,sporadic colorectal neoplasia(散発性大腸腫瘍)に支持的な所見となる3)。また,背景粘膜に強い炎症の既往を示唆する所見があれば,UC関連大腸腫瘍に支持的な所見となる7)。
一方,腫瘍性病変自体の所見から両者を鑑別する検討も行われている。本邦のエキスパートも参加して作成された分類では,病変の形態,色調,辺縁,表面構造,血管構造などを総合的に判断してUC関連大腸腫瘍を診断することを推奨している8)。しかし著者が推奨する,non-polypoid lesion,irregular vessel architecture,irregular surface pattern,病変内の潰瘍の4所見を揃えても正診率は71%(感度65%,特異度81%,陽性的中率86%,陰性的中率57%)であり,内視鏡的な両者の鑑別診断には限界があることを認識する必要がある。
SCENIC(Surveillance for Colorectal Endoscopic Neoplasia Detection and Management in Inflammatory Bowel Disease Patients:International Consensus Recommendations)では,内視鏡的に潰瘍の有無や可視病変の境界の記述などの追加情報を含む必要があると提言しているが9),treat-to-targetにより内視鏡的寛解を治療目標とする現代のUC治療ではUCの炎症による潰瘍の頻度が低下する10)。そのほかにも,UC関連大腸腫瘍に特異的な内視鏡所見として,松毬様所見や絨毛状の所見は特異度が高い所見(96.8%)として報告されているが,感度が低い(21.4%)ことに留意する必要がある11)。なお,隆起性病変周辺についても,内視鏡的に視認困難な平坦なdysplasia等の存在を念頭に,注意深い内視鏡観察と生検による確認が必要である12)。
臨床の現場では,こうした所見の有無を色素拡大内視鏡検査等で詳細に観察しながら,内視鏡的鑑別に努めることになるが,生検の病理診断でも両者の鑑別が困難な場合がありうることを考慮すると13),現状では両者の内視鏡的鑑別診断は今後の課題といえ,臨床情報も加味した総合的な鑑別が望まれる14)。なお,UC関連大腸腫瘍とUCに発生した鋸歯状病変との鑑別は今後の課題である15)。
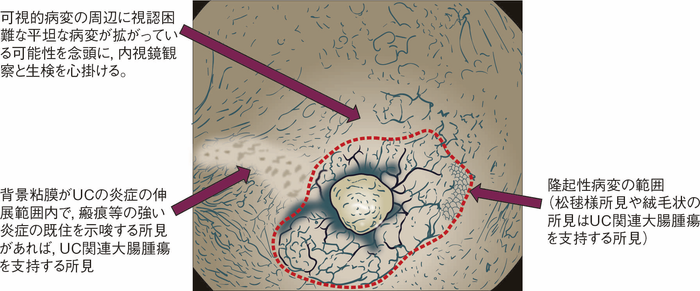
図51 UC関連大腸腫瘍の内視鏡診断
病変の形態,色調,辺縁,表面構造,血管構造などを総合的に判断して,腫瘍と非腫瘍,UC関連大腸腫瘍と散発性大腸腫瘍,との鑑別を検討する。
文献
- Kudo S, Hirota S, Nakajima T, et al.:Colorectal tumours and pit pattern. J Clin Pathol 1994;47:880-885
- Sano Y, Tanaka S, Kudo S, et al.:Narrow-band imaging(NBI)magnifying endoscopic classification of colorectal tumors proposed by the Japan NBI Expert Team. Dig Endosc 2016;28:526-533
- Iacucci M, Cannatelli R, Tontini GE, et al.:Improving the quality of surveillance colonoscopy in inflammatory bowel disease. Lancet Gastroenterol Hepatol 2019;4:971-983
- Nishiyama S, Oka S, Tanaka S, et al.:Clinical usefulness of narrow band imaging magnifying colonoscopy for assessing ulcerative colitis-associated cancer/dysplasia. Endosc Int Open 2016;4:E1183-E1187
- Matsumoto T, Iwao Y, Igarashi M, et al.:Endoscopic and chromoendoscopic atlas featuring dysplastic lesions in surveillance colonoscopy for patients with long-standing ulcerative colitis. Inflamm Bowel Dis 2008;14:259-264
- Watanabe K, Sogawa M, Yamagami H, et al.:Endoscopic differential diagnosis between ulcerative colitis-associated neoplasia and sporadic neoplasia in surveillance colonoscopy using narrow band imaging. Dig Endosc 2011;23 Suppl 1:143-149
- Mutaguchi M, Naganuma M, Sugimoto S, et al.:Difference in the clinical characteristic and prognosis of colitis-associated cancer and sporadic neoplasia in ulcerative colitis patients. Dig Liver Dis 2019;51:1257-1264
- Iacucci M, McQuaid K, Gui XS, et al.:A multimodal(FACILE)classification for optical diagnosis of inflammatory bowel disease associated neoplasia. Endoscopy 2019;51:133-141
- Laine L, Kaltenbach T, Barkun A, et al.;SCENIC Guideline Development Panel:SCENIC international consensus statement on surveillance and management of dysplasia in inflammatory bowel disease. Gastroenterology 2015;148:639-651.e28
- Turner D, Ricciuto A, Lewis A, et al.:STRIDE-Ⅱ:An Update on the Selecting Therapeutic Targets in Inflammatory Bowel Disease(STRIDE)Initiative of the International Organization for the Study of IBD(IOIBD):Determining Therapeutic Goals for Treat-to-Target strategies in IBD. Gastroenterology 2021;160:1570-1583
- Shinagawa T, Hata K, Morikawa T, et al.:Pine-cone and villi patterns are endoscopic signs suggestive of ulcerative colitis-associated colorectal cancer and dysplasia. Gastrointest Endosc 2019;89:565-575.e3
- Murthy SK, Feuerstein JD, Nguyen GC, et al.:AGA Clinical Practice Update on Endoscopic Surveillance and Management of Colorectal Dysplasia in Inflammatory Bowel Diseases:Expert Review. Gastroenterology 2021;161:1043-1051.e4
- Gui X, Iacucci M, Ghosh S, et al.:Revisiting the distinct histomorphologic features of inflammatory bowel disease-associated neoplastic precursor lesions in the SCENIC and post-DALM Era. Hum Pathol 2020;100:24-37
- Lang-Schwarz C, Adler W, Geppert M, et al.:Sporadic adenoma or ulcerative colitis associated neoplasia? The endoscopist’s information has an impact on diagnosis and patient management. Pathol Res Pract 2020;216:153-162
- Parian AM, Lazarev MG:Serrated colorectal lesions in patients with inflammatory bowel disease. Gastroenterol Hepatol(NY)2018;14:19-25
CQ 11:IBD関連消化管腫瘍に用いるべき病理診断用語・分類・基準は何か?
IBD関連消化管腫瘍の病理診断には,「Riddell system」や「厚生省(現厚生労働省)難治性炎症性腸管障害調査研究班によるUCにおける異型上皮に関する診断基準」が用いられている。
● 解説
IBDに発生した粘膜内腫瘍の診断基準として,国際的にはRiddellらによるDysplasia Morphology Study Group(DMSG)の分類(Riddell system)が広く用いられている1)。しかしながら,欧米と日本では粘膜内癌をhigh-grade dysplasia(HGD)に含めるかどうかなど組織診断基準に対する基本的な考え方の違いがあることや,Riddell systemではIBD関連粘膜内腫瘍と通常の腺腫・腺癌(散発性腫瘍)の区別がなされていない,等の問題点があることから,これらを考慮し,1994年に本邦においても,厚生省(現厚生労働省)難治性炎症性腸管障害調査研究班による基準(厚労省分類)が作成されている2)。なお,Riddell system,厚労省分類いずれも生検・切除例両方に用いられる。
以下に「Riddell system」(表7)と「厚生省(現厚生労働省)難治性炎症性腸管障害調査研究班によるUCにおける異型上皮に関する診断基準」(厚労省分類)(表8)について概説する。
本分類は国際的にも広く用いられている分類であり,IBD罹患粘膜における組織学的に異型のみられる上皮を「negative for dysplasia」,「indefinite for dysplasia」,「positive for dysplasia」と3つのカテゴリーに分類し,「positive for dysplasia」については病変の異型度に基づいて「low-grade dysplasia(LGD)」と「high-grade dysplasia(HGD)」に分類している1)。HGDには本邦において粘膜内癌と診断される病変も包含されているが,UC関連粘膜内腫瘍では,de novoの低分化型腺癌や,高・中分化腺癌で粘膜内脱分化を来す症例が少なからず認められる3)。これらの病変を他のHGDと同様に診断・対応することは過小評価につながる可能性がある。今後組織学的な悪性度をより正確に反映しうる診断基準が必要と考えられる。他方,IBDに発生した粘膜内腫瘍をすべてdysplasiaとしているため,本分類をそのまま生検組織診断に用いると,IBDに発生した散発性腺腫や腺腫内癌もdysplasiaと診断され,大腸切除される可能性があることに留意すべきである。
本分類の特徴は,日本の病理診断を考慮して,粘膜内腫瘍でも「癌」と診断できる病変を明確に区別したこと(同分類のUC-Ⅳ),「癌」と診断できないものを腫瘍性変化(UC-Ⅲ)として一括し,その中で通常の腺腫と診断しうるもの(散発性腺腫)だけを「腺腫」として分類したことが挙げられる。後者は,治療法の異なる「IBD関連粘膜内腫瘍」と「散発性腺腫」との鑑別が必要とする立場である。
世界的にはRiddell systemが汎用されているが,上述したいくつかの問題点があることから,病理診断にRiddell systemを用いる場合は,厚労省分類による診断を付記することが望ましい。


文献
- Riddell RH, Goldman H, Ransohoff DF, et al.:Dysplasia in inflammatory bowel disease:standardized classification with provisional clinical applications. Hum Pathol 1983;14:931-968
- 武藤徹一郎,若狭治毅,喜納 勇,他:潰瘍性大腸炎に出現する異型上皮の病理組織学的判定基準―surveillance colonoscopyへの応用を目的とした新判定基準の提案.日本大腸肛門病会誌1994;47:547-551
- 味岡洋一,谷 優佑,高村佳緒里,他:【大腸癌のトピックス】炎症性発癌の病理診断と発癌機序.病理と臨2018;36:1076-1081
CQ 12:IBD関連消化管腫瘍の生検病理診断において免疫染色(p53,Ki-67)は推奨されるか?
IBD関連消化管腫瘍の生検病理診断においてp53,Ki-67免疫染色を併用することは推奨される。(推奨度2・エビデンスレベルD,合意率:推奨度1;57%,推奨度2;43%)
● 解説
IBD患者の大腸内視鏡検査にて施行される生検に対する病理診断では,病勢の評価等に加えて,①腫瘍性病変の存在診断,②腫瘍性病変におけるIBD関連消化管腫瘍と散発性腫瘍との鑑別診断,が重要である。①については,高度な細胞異型・構造異型を示す浸潤癌からの生検では病理診断上問題となることは少ないが,早期病変,特にLGD,HGDに分類される粘膜内非浸潤性病変(本邦における粘膜内非浸潤癌を含む)の病理診断,特に炎症性異型を示す非腫瘍性変化との鑑別はしばしば困難である。病理医間における診断再現性の検討では,HGDと非腫瘍の鑑別では比較的良好な再現性(kappa値 0.54-0.82)がある一方で,LGDを含めた全体では再現性は比較的低い(kappa値 0.25-0.30)ことが報告されている1,2)。②については,IBD関連消化管腫瘍に特徴的な組織学的所見(CQ 13)が,内視鏡所見や臨床所見と併せて重視されるが,特に従来dysplasia-associated lesion or mass(DALM)注と呼ばれていた限局性隆起性病変の場合,IBD関連消化管腫瘍と散発性腫瘍との鑑別が困難なことがある3)。以上のことから,HE染色でIBD関連消化管腫瘍(dysplasia)と,炎症性異型あるいは散発性腺腫・散発性消化管癌との鑑別に苦慮した場合に,p53ならびにKi-67に対する免疫染色が併用される。
IBD関連消化管腫瘍の発生において,TP53遺伝子異常は極めて重要な役割を果たしており,散発性腺腫とは異なり腫瘍発生の初期から異常が生じることが知られている4-6)。2017年には,散発性大腸癌との比較で,IBD関連消化管癌におけるTP53変異の頻度が有意に高いとするメタアナリシスの結果が報告されている7)。p53蛋白に対する免疫染色も同様に,浸潤癌・dysplasiaを含むUC関連腫瘍で有用であることが2017年のメタアナリシスで示されている8)。散発性粘膜内腫瘍であっても,特に高異型度癌ではp53免疫染色で異常を認めることがあるが,UC関連粘膜内非浸潤性病変においては,陰窩深部側に限局してp53の陽性所見が認められる,“unique basal pattern”が特徴的であり,陽性細胞の分布に注目することは散発性腫瘍との鑑別に有用とする報告がある9)。なお,p53免疫染色においては,モノクローナル抗体により染色態度が異なることが知られており,評価の際には用いる抗体の特徴を理解しておくことが望ましい。例えば,DO-7はPAb1801に比べ陽性細胞頻度がより高く,染色強度がより強く表現される傾向があると報告されている10)。また,TP53変異を反映したp53免疫染色の異常所見には,強陽性細胞が連続的に出現する所見(変異型蛋白の核内蓄積が示唆される)のほかに,完全陰性所見(免疫染色で捉えられない不全型蛋白あるいは蛋白欠失が示唆される)がある11)。Ki-67が陽性となる細胞増殖領域の範囲内に弱陽性細胞が散在性に認められる場合はTP53野生型が示唆され,異常なしと判定する。
IBD関連消化管腫瘍におけるKi-67陽性細胞は,腫瘍性陰窩において粘膜深部側優位に陽性細胞が密に存在し,表層側へ向かうにつれて陽性細胞が減少する,“bottom up”と形容される分布を示すことが知られている11,12)。また,LGDでは粘膜深部側1/2に陽性細胞が留まっているのに対し,HGDや癌では表層側1/2に及ぶ傾向があると報告されている12,13)。一方,散発性腺腫では,粘膜表層側優位に陽性細胞が分布することが多く,Ki-67陽性細胞分布の評価が従来DALM注)と呼ばれていた限局性隆起性病変と散発性腺腫との鑑別に有用であるとする報告がある12,14)。これらの特徴から,IBD関連消化管腫瘍であることの判断や,LGDとHGDとの鑑別においてKi-67免疫染色の有用性が示唆される。以上より,IBD患者の内視鏡検査時に採取された生検に対する病理診断においては,HE染色に加え,p53,Ki-67免疫染色併用の有用性が示唆されるが,HE染色単独による病理診断に対する,免疫染色併用病理診断の優位性を示した大規模な研究結果の報告は無く,今後の検証が求められる。また,HE染色標本において組織形態学的に腫瘍と判断することが不可能な陰窩上皮にもp53免疫染色の異常が認められることがあると報告されている5)。現状では,HE染色標本に対する的確な組織学的評価を前提としたうえで,HE染色で疑わしい場合や鑑別困難な場合等の状況に限定して用いられる補助的役割としてp53,Ki-67免疫染色を位置づけておくことが妥当と考えられる。
注:DALMという用語は現在は使用されない。
文献
- Allende D, Elmessiry M, Hao W, et al.:Inter-observer and intra-observer variability in the diagnosis of dysplasia in patients with inflammatory bowel disease:correlation of pathological and endoscopic findings. Colorectal Dis 2014;16:710-718
- Eaden J, Abrams K, McKay H, et al.:Inter-observer variation between general and specialist gastrointestinal pathologists when grading dysplasia in ulcerative colitis. J Pathol 2001;194:152-157
- Blackstone MO, Riddell RH, Rogers BH, et al.:Dysplasia- associated lesion or mass(DALM)detected by colonoscopy in long-standing ulcerative colitis:an indication for colectomy. Gastroenterology 1981;80:366-374
- Lashner BA, Shapiro BD, Husain A, et al.:Evaluation of the usefulness of testing for p53 mutations in colorectal cancer surveillance for ulcerative colitis. Am J Gastroenterol 1999;94:456-462
- Hirsch D, Wangsa D, Zhu YJ, et al.:Dynamics of Genome Alterations in Crohn’s Disease-Associated Colorectal Carcinogenesis. Clin Cancer Res 2018;24:4997-5011
- 味岡洋一,岩永明人,渡辺 順,他:炎症性腸疾患における癌化・発育進展―潰瘍性大腸炎における大腸癌の組織発生.胃と腸2008;43:1935-1946
- Du L, Kim JJ, Shen J, et al.:KRAS and TP53 mutations in inflammatory bowel disease-associated colorectal cancer:a meta-analysis. Oncotarget 2017;8:22175-22186
- Lu X, Yu Y, Tan S. p53 expression in patients with ulcerative colitis- associated with dysplasia and carcinoma:a systematic meta-analysis. BMC Gastroenterol 2017;17:111
- Noffsinger AE, Belli JM, Miller MA, et al.:A unique basal pattern of p53 expression in ulcerative colitis is associated with mutation in the p53 gene. Histopathology 2001;39:482-492
- 横田陽子:免疫染色によるp53蛋白過剰発現の評価法について:遺伝子変異との相関からみた検討.新潟大学大学院医歯学総合研究科博士論文2015
- 味岡洋一:上皮性腫瘍に対する免疫組織化学染色―大腸上皮性腫瘍の免疫染色;UC関連腫瘍も含めて.胃と腸2017;52:1010-1018
- Mikami T, Yoshida T, Akino F, et al.:Apoptosis regulation differs between ulcerative colitis-associated and sporadic colonic tumors. Association with survivin and bcl-2. Am J Clin Pathol 2003;119:723-730
- Andersen SN, Rognum TO, Bakka A, et al.:Ki-67:a useful marker for the evaluation of dysplasia in ulcerative colitis. Mol Pathol 1998;51:327-332
- Zivković V, Petrović A, Dordević B, et al.:Computer-assisted quantitative analysis of Ki-67 antigen in dysplasia-associated lesions or masses in ulcerative colitis. Vojnosanit Pregl 2007;64:753-758
CQ 13:IBD関連消化管腫瘍と散発性腫瘍の病理所見の違いは何か?
粘膜下層以深浸潤癌
散発性腫瘍に比べ,粘液癌,低分化腺癌,印環細胞癌などの組織型の頻度が高い。
粘膜内腫瘍
IBD関連消化管腫瘍は,粘膜内脱分化,表層への細胞分化,細胞の分化異常,腺管密度増加に乏しい,粘膜全層置換,分岐の少ないストレートな腺管,周囲粘膜とのなだらかな移行,平坦な肉眼形態,bottom-up typeの細胞増殖動態,p53蛋白発現異常,を特徴とする。
● 解説
IBDに合併する粘膜下層以深浸潤癌は,散発性消化管癌に比べ,粘液癌,低分化腺癌,印環細胞癌など未分化型の癌の頻度が高い。これまでの報告ではUC,CDともにその40%前後がこれらの組織型とされている1-6)。この傾向は日本と欧米で違いはないが,CDに合併する消化管癌については,日本は欧米に比べ直腸癌特に痔瘻癌の頻度が高く,その64.5%が粘液癌であったと報告されている5)。しかしこれはIBDに合併した粘膜下層以深浸潤癌を集団としてみた場合の特徴であり,個々の症例についてその病理所見からIBDに関連した炎症性発癌病変か,炎症とは無関係に発生した散発性病変かの鑑別基準はない7)。したがって現時点ではIBDに合併する粘膜下層以深浸潤癌はすべてIBD関連消化管腫瘍とするのが現実的であるが,浸潤部に連続して明らかな散発性腺腫と診断しうる病変が併存する場合は,散発性腫瘍の可能性が高い。
IBD関連粘膜内腫瘍は,散発性粘膜内腫瘍に比べ以下のいずれか,もしくはその複数の病理所見を示すことが多い8)。
- 粘膜内低分化所見:低分化腺癌もしくは高・中分化腺癌の粘膜内低分化化9)。
- 表層への細胞分化:粘膜深層の細胞異型が最も強く表層に向かって細胞異型が弱くなる(豊富な粘液を持つ細胞に分化する)9)。
- 細胞の分化異常:内分泌細胞,パネート細胞等の豊富な分化細胞が腫瘍腺管全長にわたって出現する(pancellular change)9),核の極性が消失した異常杯細胞が多数出現する(dystrophic goblet cells)10),これらとは逆に細胞分化をほとんど示さず核クロマチンが濃染した小型円形核からなる(basal cell proliferation)9)。
- 腺管密度の増加に乏しく,腫瘍腺管が粘膜全層を置換する。
- 腫瘍腺管は比較的分岐の少ないストレートな腺管からなる。
- 周囲の非腫瘍性腺管に対して圧排性もしくは置換性発育を示さず,なだらかに移行する11)。
- 平坦な肉眼形態8)
- Ki-67染色でbottom-up typeの細胞増殖動態:Ki-67染色陽性細胞(増殖細胞)が正常陰窩と同様に腺管中層以深に高密度に出現し,表層に向かって陽性細胞頻度は減弱する(CQ 12)。
- p53免疫染色で,びまん性もしくは巣状集簇性に染色陽性となるか,完全陰性となる(CQ 12)。
①~⑥の組織学的所見および⑦~⑨の免疫染色所見からIBD関連粘膜内腫瘍とは判断されないものは散発性腫瘍と診断され,その異型度により腺腫か腺癌と診断される。Ki-67染色とp53染色はIBD関連と散発性の粘膜内腫瘍を鑑別するための有用な補助手段であるが,IBD関連粘膜内腫瘍でも異型が強くなるとKi-67染色で陽性細胞がびまん性に出現することがあること,散発性腫瘍でも癌と診断される病変ではp53蛋白過剰発現がみられること,に留意する必要がある(CQ 12)。
文献
- Mir-Madjlessi SH, Farmer RG, Easley KA, et al.:Colorectal and extracolonic malignancy in ulcerative colitis. Cancer 1986;58:1569-1574
- Heiman TM, Oh SC, Martinell G, et al.:Colorectal carcinoma associated with ulcerative colitis:a study of prognostic indicators. Am J Surg 1992;164:13-17
- Sigel JE, Petras RE, Lashner BA, et al.:Intestinal adenocarcinoma in Crohn’s disease―A report of 30 cases with a focus on coexisting dysplasia. Am J Surg Pathol 1999;23:651-655
- 鈴木公孝,渡邉聡明,畑 啓介,他:潰瘍性大腸炎の癌化とサーベイランスの検討―本邦報告例の解析―.日本大腸肛門病会誌2003;56:62-68
- 篠崎 大:クローン病と下部消化管―本邦の現況―.日本大腸肛門病会誌2008;61:353-363
- Sasaki H, Ikeuchi H, Bando T, et al.:Clinicopathological characteristics of cancer associated with Crohn’s disease. Surg Today 2017;47:35-41
- Vieth M, Neumann H:Current issues in inflammatory bowel disease neoplasia. Histopathology 2015;66:37-48
- 味岡洋一:潰瘍性大腸炎におけるcolitis-associated cancer(炎症性発癌)早期病変の病理診断―現状と問題点―.日消誌2020;117:957-964
- Riddell RH:The precarcinomatous phase of ulcerative colitis. Curr Top Pathol 1976;63:179-219
- Riddell RH, Goldman H, Ransohoff DF, et al.:Dysplasia in Inflammatory Bowel-Disease―Standardized Classification with Provisional Clinical-Applications. Hum Pathol 1983;14:931-968
- Schneider A, Stolte M:Differential diagnosis of adenomas and dysplastic lesions in patients with ulcerative colitis. Z Gastroenterol 1993;31:653-656
CQ 14:UC関連大腸腫瘍に対して大腸全摘術は推奨されるか?
- HGDおよび切除可能な大腸癌に対しては大腸全摘術が強く推奨される。(推奨度1・エビデンスレベルC,合意率:93%)
- LGDに対しては,特に癌合併のリスクが高いと考えられる場合には大腸全摘術が弱く推奨されるが(推奨度2・エビデンスレベルC,合意率:93%),腫瘍の性状よっては内視鏡切除も考慮される(CQ 21)。
● 解説
UC関連大腸腫瘍に対する大腸全摘術の有用性を他の治療法と比較したランダム化比較試験は存在しない。UC関連大腸腫瘍は同時性・異時性に多発する頻度が高く,それらを肉眼的に視認することが困難な場合も少なくない。UC関連大腸腫瘍の治療に際しては,診断時点で確認される腫瘍病変の治療に加えて,大腸の他の部位における同時性多発病変の可能性および異時性大腸腫瘍発生のリスクと患者の全身状態などを考慮する必要がある。
UC関連大腸癌における同時性多発大腸癌病変の頻度は12~30%と報告されており1-3),散発性大腸癌における頻度が2~3%3,4)であるのに対して高率である。本邦の多施設共同研究では,外科手術例406例の解析において同時性多発癌(浸潤癌)が16%に認められたと報告されている5)。
Dysplasiaの場合は,10件の前向き研究をレビューした報告によると,LGDまたはHGDが診断され,すぐに大腸切除が行われた場合に切除標本に大腸癌が診断される頻度はそれぞれ19%と42%で,一定期間経過観察の後に大腸切除が行われた場合に切除標本に大腸癌が診断される頻度はそれぞれ8%と32%であり,同時性あるいは異時性の大腸癌合併の頻度は特にHGDの場合に高率であった6)。
したがって,UC患者にHGDまたは根治切除が可能な大腸癌が診断された場合には,同時性多発病変の併存と将来の大腸癌発生リスクを考慮して大腸全摘術が推奨される。LGDの場合も同時性または異時性大腸癌の頻度は決して低くなく,得られた病理診断がLGDであるもののHGDあるいは大腸癌が強く疑われる場合には大腸全摘術を行うことを考慮する。
UCに対する大腸全摘術以外の術式として,直腸が温存される大腸亜全摘術,回腸直腸吻合術(ileorectal anastomosis:IRA)が行われるが,IRAの術後(腫瘍合併以外の適応も含む)における残存直腸からの癌発生は10年で3.2%,20年で7.3%,dysplasia発生は10年で7.1%,20年で14%と報告されており7),大腸全摘術後との比較においても有意に高いことが報告されている(OR 6.4,95%信頼区間4.3-9.5)8)。また,直腸癌発生頻度の一般人口との比較における標準化罹患比(standard incidence ratio:SIR)はIRA後で8.7,大腸亜全摘後の空置直腸で3.8と,大腸全摘,回腸囊肛門吻合術後の直腸癌のSIRが0.4であるのに比べて異時性発癌の危険性が高いことが報告されている9)。
したがって,根治切除が可能なUC関連大腸腫瘍に対する標準手術は大腸全摘術であり,特殊な状態を除いて大腸部分切除術を行わないことが推奨される。
しかしながら実際の手術術式は根治度だけでなく患者の耐術性や日常生活動作(activity of daily living:ADL),肛門機能などを総合的に判断して決定すべきであり,IBD関連大腸腫瘍か散発性腫瘍か(CQ 1,CQ 10,CQ 12),異型度(LGD,HGD,癌),局在(結腸か直腸か,単発性か多発性か),発癌のリスク因子(罹病期間,罹病範囲,PSCの合併,大腸癌家族歴など,CQ 2参照)も考慮して決定される。
高齢者,重症併存症,肛門機能低下,高度進行癌合併など特殊な状態の患者では大腸部分切除術,大腸亜全摘,回腸直腸吻合術(ileorectal anastomosis:IRA)術や大腸全摘,永久回腸人工肛門造設術も治療の選択肢となる場合がある。直腸近傍の病変に対しては,将来の括約筋機能を温存した大腸全摘術が不可能となる可能性があり低位前方切除術などの部分切除は推奨されない。
LGDの場合には,特に手術リスクの高い患者においては癌合併の頻度,癌に進展する頻度はHGDに比べて低率であることから,大腸全摘術より小範囲の切除(結腸全摘術,結腸亜全摘術,分節切除など,CQ 15参照)+内視鏡的サーベイランス,あるいは切除を行わず厳重な内視鏡的サーベイランスを行うことも選択肢として考慮される。
また,LGDに対しては,色素内視鏡検査や高画素内視鏡などによる近年のIBD関連大腸腫瘍に対する内視鏡診断能向上もあり,可能な場合には内視鏡切除を行ったうえで厳重なサーベイランスを行うstrategyも示されるようになった10)(CQ 21)。切除標本においてHGDあるいは大腸癌が認められた場合には,同時性多発病変の併存と将来の大腸癌発生リスクを考慮して大腸全摘術が推奨される。
文献
- Choi PM, Zelig MP:Similarity of colorectal cancer in Crohn’s disease and ulcerative colitis:implications for carcinogenesis and prevention. Gut 1994;35:950-954
- von Herbay A, Herfarth C, Otto HF:Cancer and dysplasia in ulcerative colitis:a histologic study of 301 surgical specimen. Z Gastroenterol 1994;32:382-388
- Greenstein AJ, Slater G, Heimann TM, et al.:A comparison of multiple synchronous colorectal cancer in ulcerative colitis, familial polyposis coli, and de novo cancer. Ann Surg 1986;203:123-128
- van Leersum NJ, Aalbers AG, Snijders HS, et al.:Synchronous colorectal carcinoma:a risk factor in colorectal cancer surgery. Dis Colon Rectum 2014;57:460-466
- Hata K, Anzai H, Ikeuchi H, et al.:Surveillance Colonoscopy for Ulcerative Colitis-Associated Colorectal Cancer Offers Better Overall Survival in Real-World Surgically Resected Cases. Am J Gastroenterol 2019;114:483-489
- Bernstein CN, Shanahan F, Weinstein WM:Are we telling patients the truth about surveillance colonoscopy in ulcerative colitis? Lancet 1994;343:71-74
- Uzzan M, Kirchgesner J, Oubaya N, et al.:Risk of Rectal Neoplasia after Colectomy and Ileorectal Anastomosis for Ulcerative Colitis. J Crohns Colitis 2017;11:930-935
- Derikx L, Nissen LHC, Smits LJT, et al.:Risk of Neoplasia After Colectomy in Patients With Inflammatory Bowel Disease:A Systematic Review and Meta-analysis. Clin Gastroenterol Hepatol 2016;14:798-806.e20
- Abdalla M, Landerholm K, Andersson P, et al.:Risk of Rectal Cancer After Colectomy for Patients With Ulcerative Colitis:A National Cohort Study. Clin Gastroenterol Hepatol 2017;15:1055-1060.e2
- Laine L, Kaltenbach T, Barkun A, et al.:SCENIC international consensus statement on surveillance and management of dysplasia in inflammatory bowel disease. Gastroenterology 2015;148:639-651.e28
CQ 15:CD関連大腸腫瘍に対して大腸部分切除は推奨されるか?
根治切除可能な大腸腫瘍に対する手術は散発性大腸癌の手術に準じ,領域リンパ節郭清を伴う大腸部分切除術が行われることが多いが,大腸部分切除術と大腸全摘術などの拡大切除と比較したエビデンスに乏しくその意義は不明である。(推奨度なし・エビデンスレベルD)
● 解説
CD関連大腸腫瘍は,術前に診断することが困難な場合も少なくない。患者の栄養状態や腫瘍以外の手術適応病変の有無,診断時点で確認される腫瘍病変の治療に加えて,大腸の他の部位における同時性多発病変の可能性と,異時性大腸腫瘍発生のリスクを考慮する必要がある。
CD関連大腸腫瘍に関する知見はUC関連大腸腫瘍に比べて限られているのが現状である。炎症からのdysplasiaを経た癌への進展経路はUC関連大腸腫瘍と同様であると考えられている1)。手術は散発性大腸癌に準じた領域リンパ節郭清を伴う腹会陰式直腸切断術や大腸部分切除術が行われているが,CD関連大腸腫瘍は同時性異時性多発病変の頻度が高いことが報告されている。欧米の報告では,dysplasiaのために大腸全摘術あるいは大腸亜全摘術をうけた患者のうち,73%の症例にHGDあるいは癌が診断され,また,44%に多発病変が検出された2)。また,大腸癌のために大腸部分切除術あるいは大腸亜全摘術を施行した患者の40%に異時性癌が診断されたことが報告されている3)。大腸部分切除術が大腸全摘,永久回腸人工肛門造設術に比べて再手術率が有意に高い(HR 5.76,95%信頼区間1.65-20.11,p=0.006)と報告されている4)。しかしながら,どのような症例がその適応になるか明確な基準はあきらかではない。本邦のCD関連大腸腫瘍の発生部位は肛門管51%,直腸29%で,直腸肛門管癌の頻度が高いのが特徴である5)。左側結腸癌の頻度はアジアでは84.1%,欧米では63.1%(p<0.01)と異なっていた6)。したがって,欧米のデータを外挿することが不可能であり,現状では蓄積されたエビデンスに乏しくその意義は不明である。
文献
- Choi PM, Zelig MP:Similarity of colorectal cancer in Crohn’s disease and ulcerative colitis:implications for carcinogenesis and prevention. Gut 1994;35:950-954
- Kiran RP, Nisar PJ, Goldblum JR, et al.:Dysplasia associated with Crohn’s colitis:segmental colectomy or more extended resection? Ann Surg 2012;256:221-226
- Maser EA, Sachar DB, Kruse D, et al.:High rates of metachronous colon cancer or dysplasia after segmental resection or subtotal colectomy in Crohn’s colitis. Inflamm Bowel Dis 2013;19:1827-1832
- Fichera A, McCormack R, Rubin MA, et al.:Long-term outcome of surgically treated Crohn’s colitis:a prospective study. Dis Colon Rectum 2005;48:963-969
- Higashi D, Katsuno H, Kimura H, et al.:Current State of and Problems Related to Cancer of the Intestinal Tract Associated with Crohn’s Disease in Japan. Anticancer Res 2016;36:3761-3766
- Uchino M, Ikeuchi H, Hata K, et al.:Intestinal cancer in patients with Crohn’s disease:A systematic review and meta-analysis. J Gastroenterol Hepatol 2021;36:329-336
CQ 16:UC関連大腸腫瘍に対する括約筋温存手術として回腸囊肛門吻合術(ileoanal anastomosis:IAA)は推奨されるか?
UC関連大腸腫瘍に対する括約筋温存手術としてIAAを行うことを弱く推奨する。(推奨度2・エビデンスレベルC,合意率:97%)
● 解説
UC関連大腸腫瘍に対する括約筋温存手術として,IAAと回腸囊肛門管吻合術(ileoanal canal anastomosis:IACA)の「生活の質(quality of life:QOL)」や長期予後を検討したランダム化比較試験は存在しない。術式の選択については患者側の要因(関連腫瘍の局在,年齢,肥満度等)も考慮しインフォームドコンセントを得たうえで行う必要がある。
UC関連大腸癌では同時多発性の病変が多いことはすでに述べられている(CQ 14)。IAAとIACAの大きな違いは肛門移行上皮帯(anal transitional zone:ATZ)の粘膜切除を行うか,温存するかである。ATZにdysplasiaが存在している頻度は2.5~4.4%と報告されている1,2)。また大腸癌合併症例の切除標本におけるATZでの癌の合併率は6.4%と報告されている3)。一方,IACA後のATZのdysplasiaや発癌症例の報告を見ると,術後10年の経過で,ATZの発癌症例は認めなかったが,dysplasiaは4.5%に認められ,そのリスク因子は,術前の内視鏡検査または切除標本で癌またはdysplasiaが認められていた症例であったとの報告がある4,5)。さらに,IACA後のATZの発癌症例の報告も増加傾向で,2017年に12例の報告があり,初回手術の手術適応が明らかになっている10症例のうち5症例の手術適応が,癌またはdysplasiaである6)。これらを考慮するとUC関連大腸腫瘍を合併する症例に対してはIAAが推奨される。
また,一方でIAAを行ったにもかかわらず,術後に発癌を生じたという症例報告も存在する7)。島状に残存した肛門管粘膜から発癌したのではないかという仮説や,明らかに歯状線近傍の粘膜が残存していたために発癌したのではないかと思われる症例もある8,9)。ただ,多くは3年以内に発癌している症例が多く,術前の直腸癌の局所再発または術前の病理診断がdysplasiaではなく癌であった可能性あるのではないかと報告されている7)。これらのことから直腸に癌またはdysplasiaを合併した症例では,IAAを行ったとしてもIACAと同様に術後に吻合部周辺のサーベイランスが必要である10)。
結腸にUC関連大腸腫瘍を合併する症例に対しては手術時の年齢,肥満度も考慮する必要がある。高齢者の手術症例は増加傾向である。術後の括約筋機能に関しては,IAAとIACAで変わらないとする報告もあるが,IACAの方が良好であるとの報告が多く,IACAの選択も説明しておくべきである11)。
また,前述したようにUC関連大腸腫瘍を合併した症例に対してはIAAが推奨されるが,体型的な問題点も考慮しなければならない12,13)。術中判断でpouchが肛門まで到達することが困難な症例では,IACA+術後のATZの内視鏡的サーベイランスという選択肢も考慮する必要がある13)。直腸に腫瘍を合併する場合はCQ 17を参照とする。
文献
- Tsunoda A, Talbot IC, Nicholls RJ:Incidence of dysplasia in the anorectal mucosa in patients having restorative proctocolectomy. Br J Surg 1990;77:506-508
- Sabayama K, Ikeuchi H, Nishigami T, et al.:Incidence of and risk factors for dysplasia in mucosectomy area in ulcerative colitis patients undergoing restorative proctocolectomy. Int J Colorectal Dis 2007;22:439-443
- Horio Y, Uchino M, Bando T, et al.:Incidence, risk factors and outcomes of cancer of the anal transitional zone in patients with ulcerative colitis. J Crohns Colitis 2020;14:1565-1571
- Remzi FH, Fazio VW, Delaney CP, et al.:Dysplasia of the anal transitional zone after ileal pouch-anal anastomosis. Results of prospective evaluation after a minimum of ten years. Dis Colon Rectum 2003;46:6-13
- Silva-Velazco J, Stocchi L, Wu XR, et al.:Twenty-year-old stapled pouches for ulcerative colitis without evidence of rectal cancer:Implications for surveillance strategy? Dis Colon Rectum 2014;57:1275-1281
- 平田晃弘,池内浩基,坂東俊宏,他:潰瘍性大腸炎に対する大腸全摘・J型回腸囊肛門管吻合術後に発症した残存肛門管癌の1例.日消外会誌2017;50:499-505
- Lee SW, Sonoda T, Milsom JW:Three cases of adenocarcinoma following restorative proctocolectomy with hand-sewn anastomosis for ulcerative colitis:a review of reported cases in the literature. Colorectal Disease 2005;7:591-597
- O’Connell PR, Pemberton JH, Weiland LH, et al.:Does rectal mucosa regenerate after ileoanal anastomosis? Dis Colon Rectum 1987;30:1-5
- Rodriguez-Sanjuan JC, Polavieja MG, Naranjo A, et al.:Adenocarcinoma in an ileal pouch for ulcerative colitis. Dis Colon Rectum 1995;38:779-780
- Block M, Börjesson L, Willén R, et al.:Neoplasia in the colorectal specimens of patients with ulcerative colitis and ileal pouch-anal anastomosis- need for routine surveillance? Scand J Gastroenterol 2015;50:528-535
- Schuender SJ, Mei L, Yang H, et al.:Can a meta-analysis answer the question:is mucosectomy and handsewn or double-stapled anastomosis better in ileal pouch-anal anastomosis? Am Surg 2006;72:912-916
- Horio Y, Uchino M, Bando T, et al.:Association between higher body mass index and pouch-related complications during restorative proctocolectomy in patients with ulcerative colitis. Digestion 2018;98:257-262
- Hardt J, Kienle P:Occult and manifest colorectal carcinoma in ulcerative colitis:How dose it influence surgical decision making? Viszeralmedizin 2015;31:252-257
CQ 17:UC関連直腸癌に対して括約筋温存手術は推奨されるか?
- UC関連の上部直腸癌に対する括約筋温存手術は弱く推奨される。(推奨度2・エビデンスレベルC,合意率:推奨度1;69%,推奨度2;24%)
- 下部直腸癌に対する括約筋温存手術は腫瘍の局在と進行度,さらに患者の希望を考慮して決定されるため,十分な術前検査とインフォームドコンセントを得たうえで行う。(推奨度なし・エビデンスレベルD)
● 解説
UC関連直腸癌に対する括約筋温存手術として,広義には内視鏡切除も含まれる。手術としてはIAA,IACAなどの括約筋温存手術と大腸全摘,永久回腸人工肛門造設術の選択が重要である。また,括約筋温存手術を目的とした下部直腸進行癌に対する術前化学放射線療法の併用も選択肢としてはあるが,症例報告レベルの報告であり,推奨には言及できない(CQ 26)。
UC関連大腸腫瘍に関する内視鏡治療は,正確な病理診断を目的としたtotal biopsyの意味での内視鏡切除を否定することはできない。ただ,UCでは内視鏡的粘膜下層剝離術(endoscopic submucosal dissection:ESD)時に97%の症例で,すでに粘膜下層の繊維化が進行していると報告されている1)。このため下部直腸の早期癌やHGDに対する内視鏡切除は,その後,手術が必要となった場合,肛門測からの直腸粘膜切除部への影響もあり,括約筋機能の低下が懸念される。そのため,治療的意義での推奨には言及できない(CQ 21)。
UC関連の上部直腸癌に対する治療は,結腸にUC関連大腸腫瘍を合併する症例と同様に考えて問題ない。UC関連直腸癌を上部直腸に合併する場合にはIACAよりもIAAが強く推奨される(CQ 16)2,3)。また,IAAが体型的に困難な症例ではIACA+術後の内視鏡的サーベイランスという選択肢も否定することはできない。
UC関連大腸癌は,散発性大腸癌に比べ,腫瘍組織と非腫瘍組織の区別が不明確であり,下部直腸癌に対する手術では,肛門側切離端が陽性となる可能性がある4,5)。また,腫瘍周囲のdysplasiaの存在も術式選択を複雑にする。
術式の選択としてはIAAまたは大腸全摘,永久回腸人工肛門造設術の選択となる。どちらを選択するかは患者サイドの希望に左右されることも多い。また,UCに合併する下部直腸癌の術前治療や,術式,予後に関する報告は少なく,最も多い症例数の報告でも41例の報告であり,文献的な裏付も不十分である6)。そのため,術式を推奨することは困難である。
また,散発性の直腸癌と同様に術前化学放射線療法を行った後IAAを行った症例や括約筋間直腸切除術(intersphincteric resection:ISR)をともなうIAAを行った症例もあるものの,少数例の報告に過ぎず,推奨することはできない7,8)。
いずれにしてもUC関連下部直腸癌に対する括約筋温存手術に関する報告には限界があり,術式を推奨できるレベルには達していない。術式選択は,術前の病理診断,患者の年齢,パフォーマンスステータス,個人的な優先順位なども考慮し,十分なインフォームドコンセントを得たうえで行うべきである4)。
文献
- Suzuki N, Toyonaga T, East JE:Endoscopic submucosal dissection of colitis-related dysplasia. Endoscopy 2017;49:1237-1242
- Remzi FH, Fazio VW, Delaney CP, et al.:Dysplasia of the anal transitional zone after ileal pouch anal anastomosis:results of prospective evaluation after minimum of the ten years. Dis Colon Rectum 2003;46:6-13
- Hardt J, Kienle P:Occult and manifest colorectal carcinoma in ulcerative colitis:How does it influence surgical decision making? Viszeralmedizin 2015;31:252-257
- Senis B, Bagaglini G, Bellato V, et al.:Management of low rectal cancer complicating ulcerative colitis:Proposal of a treatment algorithm. Cancers(Basel)2021;13:2350
- Hotta S, Shimada Y, Nakano M, et al.:Feasibility of restorative proctocolectomy in patients with ulcerative colitis-associated lower rectal cancer;A retrospective study. Asian J Surg 2019;42:267-273
- Merchea A, Wolff BG, Dozois EJ, et al.:Clinical features and oncologic outcomes in patients with rectal cancer and ulcerative colitis:a single-institution experience. Dis Colon Rectum 2012;55:881-885
- Gorfine SR, Harris MT, Bub DS, et al.:Restorative proctocolectomy for ulcerative colitis complicated by colorectal cancer. Dis Colon Rectum 2004;47:1377-1385
- Inoue Y, Araki T, Okugawa Y, et al.:Chemoradiotherapy followed by restorative proctocolectomy with partial intersphincteric resection for advanced rectal cancer associated with ulcerative colitis:Report of a case. Surg Today 2013;44:387-390
CQ 18:CD関連直腸肛門管癌に対する最適な術式は何か?
CD関連直腸肛門管癌に対する術式について,予後や合併症などを含めた治療成績のエビデンスレベルの高い報告はないものの,実臨床では腹会陰式直腸切断術が行われることが多い。(推奨度なし・エビデンスレベルD)
● 解説
CD関連直腸肛門管癌に対する術式は,基本的には一般大腸癌に準じるが,CD関連消化管癌の特徴を理解した選択が必要になる。エビデンスレベルの高い多数例での検討は少ないものの,本邦報告が参考となる。
CDには痔瘻をはじめとする肛門病変の合併例が多い。粘液癌の頻度が高く,CD関連消化管癌122例を集計した本邦報告でも50%と高く1),直腸肛門管癌のみでみてもレビューでは30~54%と報告されている2,3)。壁深達度はCD関連消化管癌のシステマティックレビューでは直腸肛門管癌でT3以上が62%と報告され4),前出のCD関連消化管癌例の集計報告でも筋層以深が91%と報告されており1),進行癌が多い。
これらの特徴から,術式は腹会陰式直腸切断術が選択される場合が最も多く3),CD関連消化管癌の集計報告でも67%に行われていた1)(CQ 14)。また,痔瘻癌を含め,直腸周囲組織への浸潤例が多く,外科的剝離面の断端陰性の確保が困難で癌遺残となる症例は29%(24例中7例)と多いとされており(単施設の報告)2),剝離断端の確保のため骨盤内臓全摘術が行われる場合もある3)。
直腸低位で吻合を行う括約筋温存手術(括約筋間直腸切除術を含む)は,CDでは腸管病変自体の術後再発率が高く,再手術の責任病変は手術施行部に存在することが80%と最も多く5),再発予防として行われる免疫を抑制する治療の可否は癌再発への影響を十分に考慮して判断する必要があることから6),選択には慎重な検討が必要と考えられる。
直腸を温存するHartmann手術を選択する際にもCDの腸管吻合では縫合不全の発生率が2.2~4.3%と比較的高いため7,8),直腸断端の縫合不全などの合併症や空置部に発癌がある可能性9)を十分に考慮する必要があると考えられる。
本症に対する術式に関しては,大腸全摘術の意義は不明で(CQ 14),他臓器合併切除や骨盤内臓全摘術などの適否を含め,今後の検討が必要である。
文献
- Higashi D, Katsuno H, Kimura H, et al.:Current state of and problems related to cancer of the intestinal tract associated with Crohn’s disease in Japan. Anticancer Res 2016;36:3761-3766
- Sasaki H, Ikeuchi H, Bando T, et al.:Clinicopathological characteristics of cancer associated with Crohn’s disease. Surg Today 2017;47:35-41
- 杉田 昭,小金井一隆,辰巳健志,他:クローン病に合併する直腸肛門管癌.日消誌2013;110:396-402
- Uchino M, Ikeuchi H, Hata K, et al.:Intestinal cancer in patients with Crohn’s disease:A systematic review and meta-analysis. J Gastroenterol Hepatol 2021;36:329-336
- 二見喜太郎,東 大二郎,二木 了,他:クローン病の長期経過における外科の役割と術後再発予防の戦略.日消誌2011;108:410-417
- 厚生労働科学研究費補助金 難治性腸管疾患政策研究事業「難治性戦傷性腸管障害に関する調査研究」(久松班).クローン病治療指針.潰瘍性大腸炎・クローン病 診断基準・治療指針 令和2年度分担研究報告書,2021:30-36
- 桑原隆一,池内浩基,皆川知洋,他:クローン病に対する腸管切除症例1,143例の検討.日消外会誌.2018;51:671-679
- 東 大二郎,二見喜太郎,永川祐二,他:Crohn病における縫合不全の予防と対策.日本大腸肛門病会誌2009;62:818-822
- Kuroki H, Sugita A, Koganei K, et al.:Clinicopathological and prognostic evaluations of anorectal cancer after fecal diversion for patients with Crohn’s disease. BMC Gastroenterol 2021;21:168
CQ 19:CD関連小腸癌に対する最適な術式は何か?
- リンパ節郭清を伴った小腸部分切除術ないしは回結腸切除術を行うことを弱く推奨する。(推奨度2・エビデンスレベルD,合意率:86%)
- CD関連小腸癌は術前に診断できることが少ないため,臨床経過や術中所見から積極的に癌を疑う場合には術中迅速組織診断を行うことを考慮する。(推奨度なし・エビデンスレベルD)
● 解説
CD関連小腸癌はまれであることに加えて術前に診断されることが少ないため,術式ごとの成績を比較した研究は存在しない。CD関連小腸癌は,空腸に好発する一般的な小腸癌とは異なり回腸に好発することが知られており1-7),手術は通常,小腸部分切除術か回結腸切除術が行われる1,2)。米国のSurveillance, Epidemiology and End Results(SEER)cancer registry-Medicare linked databaseより抽出されたCD関連小腸癌179例を含む小腸癌患者2,123例を対象とした大規模後ろ向き研究によれば,CD関連小腸癌と一般的な小腸癌の間で全生存期間(overall survival:OS)に差はないが,リンパ節検索個数が多いほどOSが有意に良好であることが多変量解析により示され,リンパ節検索個数0個に対する10~19個のHRが0.51(95%信頼区間0.42-0.61,p<0.0001)であった3)。また単施設のCD関連小腸癌29例という少数例での検討であるが,リンパ節転移陰性例では2年生存率が79%であったのに対し,転移陽性例では49%と有意に予後が悪いことが示された1)。CD関連小腸癌においても通常の大腸癌と同様,リンパ節転移が予後規定因子となりうると考えられ,十分なリンパ節郭清が予後改善につながる可能性が高い。なお,小腸癌において郭清対象とする領域リンパ節についてはこれまでエビデンスに基づいた定義がなされてはおらず,腸管切除範囲についても明確な推奨がないのが現状である。
しかしながらCD関連小腸癌は前述のごとく術前に診断されることが少なく,術中あるいは術後の病理診断で偶発的に発見される症例の比率が79~100%と高いことがこれまで報告されている1,2,5-7)。CDに対する腸切除術においては栄養の吸収に関わる小腸を十分に温存することが重視されることから,手術時までに小腸癌の診断がなされていないと十分な領域リンパ節郭清が行われないという問題がある。このため,臨床経過や術中所見から癌が疑われる場合には,術前に小腸癌の診断がついていなくても積極的に術中迅速組織診断を行い,術中に癌と診断されれば十分な領域リンパ節郭清を行うという治療戦略がCD関連小腸癌の治療成績向上に寄与する可能性がある2,5)。癌を疑う臨床経過や術中所見としては,これまで以下のようなものが提唱されている。すなわち臨床経過としては,内科治療で改善しない腸閉塞症状,入院を要するような強い再発症状の前に長期の寛解期間があることが挙げられている1)。また術中所見としては,以前の狭窄形成部が硬く触知されること,慢性の瘻孔,大網や間膜の結節形成,硬く複雑な小腸の腫瘤形成が挙げられている2)。
文献
- Widmar M, Greenstein AJ, Sachar DB, et al.:Small bowel adenocarcinoma in Crohn’s disease. J Gastrointest Surg 2011;15:797-802
- Hussain T, Jeganathan NA, Karagkounis G, et al.:Small bowel adenocarcinoma in Crohn’s disease:a rare but devastating complication. Tech Coloproctol 2020;24:1055-1062
- Wieghard N, Mongoue-Tchokote S, Young JI, et al.:Prognosis of small bowel adenocarcinoma in Crohn’s disease compares favourably with de novo small bowel adenocarcinoma. Colorectal Dis 2017;19:446-455
- Fields AC, Hu FY, Lu P, et al.:Small Bowel Adenocarcinoma:Is There a Difference in Survival for Crohn’s Versus Sporadic Cases? J Crohns Colitis 2020;14:303-308
- Svrcek M, Piton G, Cosnes J, et al.:Small bowel adenocarcinomas complicating Crohn’s disease are associated with dysplasia:a pathological and molecular study. Inflamm Bowel Dis 2014;20:1584-1592
- Cahill C, Gordon PH, Petrucci A, et al.:Small bowel adenocarcinoma and Crohn’s disease:any further ahead than 50 years ago? World J Gastroenterol 2014;20:11486-11495
- 篠崎 大.クローン病と下部消化管癌―本邦の現況―.日本大腸肛門病会誌2008;61:353-363
CQ 20:IBD関連消化管癌に対する低侵襲手術は推奨されるか?
IBD関連消化管癌に対して腹腔鏡下手術を行うことを弱く推奨する。(推奨度2・エビデンスレベルD,合意率:90%)ただし手術難度は高く,個々の手術チームの習熟度を十分に考慮して適応を決定する。
● 解説
IBD関連消化管癌に対する低侵襲手術の有用性に関する確立したエビデンスはない。IBDの外科的治療に関するいくつかの海外のガイドラインにおいても,IBD関連消化管癌に対する低侵襲手術の有用性について言及されていない1,2)。そのため,類似疾患に対する低侵襲手術のガイドラインや手術成績を参考にする必要がある。
日本内視鏡外科学会のアンケート調査によれば3),2019年までの低侵襲手術症例数は,UC 3,974例,CD 3,631例であり,そのほとんどすべては腹腔鏡下手術により行われたと思われる。IBDに対する低侵襲手術の多くは内科治療不応性の症例に対する手術であることを考慮すると,IBD関連消化管癌に対する低侵襲手術は非常に限られた症例に対して行われていると考えられる。
散発性大腸癌に対してはすでに多くの施設で低侵襲手術が行われている現状がある。その経験をもとに実地臨床ではIBD関連消化管癌に対しても低侵襲手術の導入が行われているものと思われるが,その手術成績の詳細については明らかでない。IBDに対するロボット手術については世界的に見ても少数例のケースシリーズがあるだけであり,IBD関連消化管癌にどのようにロボット手術を応用するのかついては今後の研究課題であると考えられる。
疾患の希少性からは大規模ランダム化比較試験を行って,低侵襲手術の有用性を明らかにすることは現実的ではない。術者の技量や疾患の特徴をしっかりと把握し,十分なインフォームドコンセントを行ったうえで慎重に低侵襲手術を行うことを推奨する。
UC関連大腸癌
UC関連大腸癌を認めた場合の標準手術は大腸全摘術であるが,リンパ節郭清を伴う腹腔鏡下大腸全摘術を行った場合の周術期の安全性と腫瘍学的な根治性に関する報告はない。「遺伝性大腸癌診療ガイドライン 2020年版」では,大腸癌を合併した際に同じく大腸全摘術が行われる家族性大腸腺腫症に対しては,腹腔鏡下手術を弱く推奨するとしている4)。一方で,海外および本邦のガイドラインでは,薬物療法不応性のUCに対する大腸全摘術には,腹腔鏡下手術が推奨されている1,2,5)。
大腸全摘術に対する腹腔鏡下手術と開腹手術を比較した27件の観察研究を中心とするメタアナリシスによれば6),腹腔鏡下手術は開腹手術と比較して手術時間を約70分延長し,出血量を約90 g減少させた。また,創感染を約40%抑制し,術後在院日数を約1日短縮させ,排便機能も改善させた。その他,腹腔鏡下手術においては腹腔内癒着強度が減少し7),QOLに関するスコアが良好であることが報告されている8)。一方で,ロボット手術に関する報告は少ない。ロボットを用いた大腸全摘術に関するシステマティックレビューによれば,大腸全摘術の中でロボットが使われるのは直腸切除術のみであり,結腸全摘術は腹腔鏡下手術で行われたとの報告が多い9)。術後合併症については,後ろ向き観察研究において腹腔鏡下手術とほぼ同等であると報告されている10)。経肛門的直腸切除術と腹腔鏡下手術の併用術式についても報告は少ないが,腹腔鏡下手術のみで行われた手術とQOLにおいて同等であると報告されている11)。いずれの研究もUC関連大腸癌に対する研究でないことに注意されたい。
その他手技上の注意点として,右側結腸癌を認めた場合の回結腸動脈の温存や,横行結腸癌を認めた場合の横行結腸間膜のエネルギーデバイスによる一括処理等は,リンパ節郭清不足につながる可能性があることが挙げられる。また,直腸癌に対する腹腔鏡下手術は手術の質が開腹手術に劣る傾向があるとの最近の報告12,13)もあり,低侵襲手術は十分に経験を積んだ施設で行われるべきである。
CD関連消化管癌
CDは大腸だけでなく,小腸や肛門部にも発癌することがあり,術式も非常に多彩である。CD関連消化管癌に低侵襲手術を行った場合の周術期の安全性と腫瘍学的な根治性に関する報告はない。海外および本邦のガイドラインでは,CDに対して腹腔鏡下手術を行うことを推奨しているが,複雑な病変や再発の病変については専門家が手術すべきとの論調である5,14,15)。CD関連消化管癌は複雑な病変と考えられ,慎重に腹腔鏡下手術の適応を考えなければならない。
CD関連消化管癌に対する標準手術は原発巣切除および領域リンパ節郭清である。すなわち,手術の原則は散発性消化管癌と同様であり,その結果をある程度参考にすることができる。以下,術後成績と腫瘍学的観点に分けて述べる。
術後成績としては以下の報告が参考になる。CDに対する低侵襲手術の研究は,ほとんどが回盲部病変に関するものである。いくつかのランダム化比較試験で,腹腔鏡下手術は開腹手術と比較して,入院期間の短縮,合併症の減少,費用の削減が見込まれると報告されている16,17)。傾向スコアマッチングを用いてロボット手術と開腹手術を比較した研究によれば,ロボット手術は合併症の減少と在院日数の短縮に寄与すると報告されている18)。
腫瘍学的観点からは以下の報告が参考になる。小腸癌に対する低侵襲手術の報告はないが,病期診断のためには9個以上のリンパ節を切除・検索すべきとの報告があり19),低侵襲手術においてもこの数字を満たすようにリンパ節郭清をしなければならない。大腸癌に対する低侵襲手術については,開腹手術と腹腔鏡下手術を比較したいくつかのランダム化比較試験の報告があり,長期成績において腹腔鏡下手術は開腹手術とほぼ同等であると報告され20,21),腹腔鏡下手術が広く行われている。
特にCD関連小腸癌は,術前に診断がつくことが少なく,触覚のない腹腔鏡下手術では術中に癌の存在を疑うことも難しいことを念頭におきながら手術を行う必要がある。また,痔瘻癌においては触覚のない低侵襲手術では十分な瘻孔の切除を行うことができない可能性があり,病変の広がりと術者の技量をしっかりと把握し,低侵襲手術によって癌の根治性が損なわれることがあってはならない。
文献
- Spinelli A, Bonovas S, Burisch J, et al.:ECCO Guidelines on Therapeutics in Ulcerative Colitis:Surgical Treatment. J Crohns Colitis 2021;16:179-189
- Holubar SD, Lightner AL, Poylin V, et al.;Prepared on behalf of the Clinical Practice Guidelines Committee of the American Society of Colon and Rectal Surgeons:The American Society of Colon and Rectal Surgeons Clinical Practice Guidelines for the Surgical Management of Ulcerative Colitis. Dis Colon Rectum 2021;64:783-804
- 日本内視鏡外科学会学術委員会編:内視鏡外科手術に関するアンケート調査―第15回集計結果報告―,一般社団法人日本内視鏡外科学会,東京,2021:149
- 大腸癌研究会編:遺伝性大腸癌診療ガイドライン2020年版,金原出版,東京,2020:133
- 日本内視鏡外科学会編:技術認定取得者のための内視鏡外科学会ガイドライン2019年度版_06大腸領域
- Singh P, Bhangu A, Nicholls RJ, et al.:A systematic review and meta-analysis of laparoscopic vs open restorative proctocolectomy. Colorectal Dis 2013;15:e340-e351
- Hull TL, Joyce MR, Geisler DP, et al.:Adhesions after laparoscopic and open ileal pouch-anal anastomosis surgery for ulcerative colitis. Br J Surg 2011;99:270-275
- Lavryk OA, Stocchi L, Ashburn JH, et al.:Case-Matched Comparison of Long-Term Functional and Quality of Life Outcomes Following Laparoscopic Versus Open Ileal Pouch-Anal Anastomosis. World J Surg 2018;42:3746-3754
- Flynn J, Larach JT, Kong JCH, et al.:Robotic versus laparoscopic ileal pouch-anal anastomosis(IPAA):a systematic review and meta-analysis. Int J Colorectal Dis 2021;36:1345-1356
- Lightner AL, Grass F, McKenna NP, et al.:Short-term postoperative outcomes following robotic versus laparoscopic ileal pouch-anal anastomosis are equivalent. Tech Coloproctol 2019;23:259-266.
- Chandrasinghe P, Carvello M, Wasmann K, et al.:Transanal Ileal Pouch-Anal Anastomosis for Ulcerative Colitis has Comparable Long-Term Functional Outcomes to Transabdominal Approach:A Multicentre Comparative Study. J Crohns Colitis 2020;14:726-733
- Fleshm an J, Branda M, Sargent DJ., et al.:Effect of Laparoscopic-Assisted Resection vs Open Resection of Stage II or III Rectal Cancer on Pathologic Outcomes:The ACOSOG Z6051 Randomized Clinical Trial. JAMA 2015;314:1346-1355
- Stevenson A, Solomon MJ, Lumley JW, et al.:Effect of Laparoscopic-Assisted Resection vs Open Resection on Pathological Outcomes in Rectal Cancer:The ALaCaRT Randomized Clinical Trial. JAMA 2015;314:1356-1363
- Bemelman WA, Warusavitarne J, Sampietro GM, et al.:ECCO-ESCP Consensus on Surgery for Crohn’s Disease. J Crohns Colitis 2018;12:1-16
- Lightner AL, Vogel JD, Carmichael JC, et al.:The American Society of Colon and Rectal Surgeons Clinical Practice Guidelines for the Surgical Management of Crohn’s Disease. Dis Colon Rectum 2020;63:1028-1052
- Maartense S, Dunker MS, Slors JFM, et al.:Laparoscopic-assisted versus open ileocolic resection for Crohn’s disease:a randomized trial. Ann Surg 200;243:143-149;discussion 150-153
- Milsom JW, Hammerhofer KA, Böhm B, et al.:Prospective, randomized trial comparing laparoscopic vs. conventional surgery for refractory ileocolic Crohn’s disease. Dis Colon Rectum 2001;44:1-8;discussion 8-9
- Raskin ER, Gorrepati ML, Mehendale S, et al.:Robotic-assisted ileocolic resection for Crohn’s disease:outcomes from an early national experience. J Robot Surg 2019;13:429-434
- Tran TB, Qadan M, Dua MM, et al.:Prognostic relevance of lymph node ratio and total lymph node count for small bowel adenocarcinoma. Surgery. 2015;158:486-493
- Kitano S, Inomata M, Mizusawa J, et al.:Survival outcomes following laparoscopic versus open D3 dissection for stage Ⅱ or Ⅲ colon cancer(JCOG0404):a phase 3, randomised controlled trial. Lancet Gastroenterol Hepatol. 2017;2:261-268
- Bonjer HJ, Deijen CL, Haglind E;COLOR Ⅱ Study Group:A Randomized Trial of Laparoscopic versus Open Surgery for Rectal Cancer. N Engl J Med 2015;373:194
CQ 21:UC関連大腸腫瘍に対して内視鏡切除は推奨されるか?
- 内視鏡切除に関する安全性および長期予後に関するエビデンスはないが,UC関連大腸腫瘍と散発性腫瘍との鑑別をすることは容易ではないため,境界明瞭な病変については診断確定のために内視鏡切除を行うことが考慮される。(推奨度なし・エビデンスレベルD)ただし,生検でHGDないし癌と診断がついているものは原則大腸全摘術が推奨される。また,内視鏡切除後の病理診断でHGDもしくは癌と診断された場合も原則大腸全摘術が推奨される(CQ 14)。
- 内視鏡切除を行う場合,境界明瞭な病変に対しては治癒切除の観点から,内視鏡的粘膜下層剝離術(endoscopic submucosal dissection:ESD)や内視鏡的粘膜切除術(endoscopic mucosal resection:EMR)などでの一括切除を行うことが推奨されるが,大腸腫瘍に対する内視鏡切除に熟練した内視鏡医により施行されることが望ましい。(推奨度なし・エビデンスレベルD)
- 境界不明瞭なUC関連大腸腫瘍については,内視鏡切除は行わないことが推奨される。(推奨度2・エビデンスレベルD,合意率:推奨度1;58%,推奨度2;27%)
● 解説
UC関連大腸腫瘍に対する内視鏡切除の有用性を他の治療法と比較したランダム化比較試験は存在しない。SCENIC(Surveillance for Colorectal Endoscopic Neoplasia Detection and Management in Inflammatory Bowel Disease Patients:International Consensus Recommendations)では,腫瘍病変の境界が明瞭である病変に対しては内視鏡切除の適応であるとされている1)。またAmerican College of Gastroenterologyのexpert reviewでは浸潤癌の徴候や顕著な粘膜下層の線維化を伴わない,境界が明瞭なdysplasia病変はすべて内視鏡切除を考慮すべきであるとされている2)。しかしこれらステートメントの根拠となっている研究は慢性炎症を母地としたUC関連大腸腫瘍と散発性腫瘍とを区別して検討されていない点を理解する必要がある。またコンセンサスステートメントの根拠はポリペクトミーもしくはEMRの治療成績をもとにした研究であることに留意する必要がある3)。なお本邦のEMR/ESDガイドラインでは,UC関連大腸腫瘍に対する内視鏡切除は推奨されていない4)。
SCENICの根拠となった9つの研究結果よりUC患者における隆起性病変に対するEMRもしくはスネアを用いたポリペクトミーの治療成績は,フォローアップ時の大腸癌への進展や再発率はかなり低かったとされているものの,内視鏡切除後のいくつかの研究は,散発性腺腫(内視鏡切除可能)の割合が50%程度に達していることより,治療後のサーベイランスが必要であると考えられる1)。一方で非隆起性病変に対するEMRについては治療後の再発率を検討した明確な研究がないこと1),範囲診断と深達度診断に限界があること,線維化が強く技術的に困難であり,分割切除や非治癒切除になる可能性が高いこと5,6)より,EMRもしくはポリペクトミーは施行されないことが推奨される。
UC関連大腸腫瘍に対するESDの治療成績に対する研究は存在しない。報告されているすべての論文は,UC関連大腸腫瘍と散発性腫瘍の両者を含む,UCに合併した大腸腫瘍に関する研究内容である可能性が高いことを勘案して,結果を解釈する必要がある。コホート研究の報告例7-12)では,ESDの一括切除術は比較的高いが,粘膜下層の線維化や脂肪沈着が認められることが多いため7-8),治療には高度な技術が必要とされる。ケースシリーズにおいて,大腸全摘術後の残存粘膜に発生した腫瘍病変に対してESDを施行し治癒切除可能であった報告もされている13)。
UCに合併した大腸腫瘍に対するESDの有用性と安全性に関して2つのシステマティックレビューがなされているが12,14),システマティックレビューに使用された研究は上述したようにUC関連大腸腫瘍と散発性腫瘍を区別して検討されていない。Mantaらは本邦と欧州の6研究の208例,216病変についてシステマティックレビューを行い,病変に対するR0切除率,一括切除率はそれぞれ78.2%(95%信頼区間 72.3-83.2%),88.4%(95%信頼区間 83.5-92.0%)であることを報告している13)。合併症としては出血率6.7%,穿孔率は2.9%であること,再発については,局所再発が3.8%,異所性再発が6.2%あることを報告している12)。しかしこのシステマティックレビューは各個研究のバイアスリスク評価や研究間の非一貫性,不正確性に関する評価は行われておらず,エビデンスとしては極めて弱いと考えられる。Chenらは非隆起性病変に対する7研究,202例の内視鏡切除の治療成績,予後について検討し,R0切除率,一括切除率はそれぞれ0.70(95%信頼区間 0.55-0.81)と0.86(95%信頼区間 0.65-0.95)であり,再発率は0.08(95%信頼区間 0.05-0.13)であることを報告している。本研究のメタアナリシスではUCに合併した大腸癌および異時性dysplasiaの発生率は,1,000患者/年あたり32.53(95%信頼区間 12.21-86.67)および90.24(95%信頼区間 44.91-181.33)であった14)。
内視鏡下生検による病理診断では癌,HGD,LGDの鑑別が容易ではないこともあるため,境界が明瞭な病変に対しては,正確な病理診断を目的とした内視鏡切除が行われることがあるが,高度な技術を要することより大腸腫瘍に対する内視鏡切除に熟練した専門医により施行されるべきである。内視鏡切除の適応病変として,表面潰瘍のない,明確な境界な病変,粘膜下への局注により良好なliftingが認められること9),深部浸潤がないこと,粘膜下層に著明な線維化がないこと15)が挙げられている。また内視鏡切除後に同時性,異時性再発が一定の確率で出現することより,定期的な内視鏡的サーベイランスを施行する必要がある(CQ 22)。
現時点ではR0切除であっても切除周囲に病変(平坦型が多い)が認められることがあるため,経験豊富な病理医へのコンサルトとともに,慎重に経過観察をする必要がある。また内視鏡切除後に病理診断でHGDもしくは大腸癌と診断された場合には,原則として大腸全摘術が推奨される(CQ 14)。
文献
- Laine L, Kaltenbach T, Barkun A, et al.:SCENIC international consensus statement on surveillance and management of dysplasia in inflammatory bowel disease. Gastrointest Endosc 2015;81:489-501
- Murthy SK, Feuerstein JD, Nguyen GC, et al.:AGA Clinical Practice Update on Endoscopic Surveillance and Management of Colorectal Dysplasia in Inflammatory Bowel Diseases:Expert Review. Gastroenterology 2021;161:1043-1051. e4
- 松本主之,川崎啓祐:潰瘍性大腸炎に対するサーベイランス―SCENIC international consensus statementの概要と問題点.胃と腸2020;55:191-199
- Tanaka S, Kashida H, Saito Y, et al.:Japan Gastroenterological Endoscopy Society guidelines for colorectal endoscopic submucosal dissection/endoscopic mucosal resection. Dig Endosc 2020;32:219-239
- Kinoshita S, Nishizawa T, Yahagi N, et al., Endoscopic Submucosal Dissection in Patients with Ulcerative Colitis. Digestion 2019;99:27-32
- 浦岡俊夫,橋本 悠,佐藤圭吾,他:潰瘍性大腸炎関連腫瘍に対する内視鏡治療―私はこう考える.胃と腸2020;55:170-171
- Iacopini F, Saito Y, Yamada M, et al.:Curative endoscopic submucosal dissection of large nonpolypoid superficial neoplasms in ulcerative colitis(with videos). Gastrointest Endosc 2015;82:734-738
- Suzuki N, Toyonaga T, East JE:Endoscopic submucosal dissection of colitis-related dysplasia. Endoscopy 2017;49:1237-1242
- Kinoshita S, Uraoka T, Nishizawa T, et al.:The role of colorectal endoscopic submucosal dissection in patients with ulcerative colitis. Gastrointest Endosc 2018;87:1079-1084
- Yang DH, Kim J, Song EM, et al.:Outcomes of ulcerative colitis-associated dysplasia patients referred for potential endoscopic submucosal dissection. J Gastroenterol Hepatol 2019;34:1581-1589
- Matsumoto K, Oka S, Tanaka S, et al.:Long-Term Outcomes after Endoscopic Submucosal Dissection for Ulcerative Colitis-Associated Dysplasia. Digestion 2021;102:205-215
- Manta R, Zullo A, Telesca DA, et al.:Endoscopic submucosal dissection for visible dysplasia treatment in ulcerative colitis patients:Cases series and systematic review of literature. J Crohns Colitis 2021;15:165-168
- Yoshii S, Shinzaki S, Hayashi Y, et al.:Endoscopic submucosal dissection for remnant rectal neoplasm after ileal pouch-anal anastomosis for ulcerative colitis. Endoscopy 2019;51:E406-E407
- Chen W, Zhang YL, Zhao Y, et al.:Endoscopic resection for non-polypoid dysplasia in inflammatory bowel disease:a systematic review and meta-analysis. Surg Endosc 2021;35:1534-1543
- Murthy SK, Feuerstein JD, Nguyen GC, et al.:AGA Clinical Practice Update on Endoscopic Surveillance and Management of Colorectal Dysplasia in Inflammatory Bowel Diseases:Expert Review. Gastroenterology 2021;161:1043-1051
CQ 22:UC関連大腸腫瘍に対する内視鏡切除後の最適なサーベイランス法は何か?
UC関連大腸腫瘍に対する内視鏡切除後は大腸内視鏡検査によるサーベイランスが考慮されるが,内視鏡切除後のサーベイランスの間隔や色素散布法・画像強調内視鏡の併用によるサーベイランス法の有効性は明らかではない。(推奨度なし・エビデンスレベルD)
● 解説
UC関連大腸腫瘍に対して内視鏡切除後にdysplasiaや大腸癌が検出されることが報告されている1-5)。近年報告された内視鏡切除された208例,216病変を対象としたシステマティックレビューでは,治療後に8例(3.8%,95%信頼区間 2.0-7.4%),13病変(6.2%,95%信頼区間 3.7-10.4%)の異時性再発が認められている6)。現時点ではR0切除であっても,内視鏡切除後に病理診断でHGDもしくは大腸癌と診断された場合には原則として大腸全摘術が推奨される。LGDの場合はHGDに比べて同時性・異時性大腸癌のリスクは相対的には低率であることより,内視鏡切除後に大腸全摘術を行わずに定期的な大腸内視鏡検査によるサーベイランスを行うことが考慮される。
内視鏡的粘膜切除術(endoscopic mucosal resection:EMR)やポリペクトミーを中心とした376例の隆起病変に対する内視鏡切除後の予後は,平均54カ月の観察期間で大腸癌発生率は1年間で0.5%であり7),SCENIC(Surveillance for Colorectal Endoscopic Neoplasia Detection and Management in Inflammatory Bowel Disease Patients: International Consensus Recommendations)では隆起性病変に対して内視鏡的治癒切除がされた場合には,大腸全摘術よりサーベイランスによる経過観察を強く推奨している8)。その場合サーベイランス間隔に関しては,隆起性病変に対して内視鏡切除を施行した場合には3~6カ月に大腸内視鏡検査を行い,もし病変が検出されなかった場合にはその後はより間隔をあけたサーベイランスが考慮される。推奨の対象となる病変にはUC関連大腸腫瘍であるLGDと散発性腺腫が混在していると考えられるが,両者の区別は困難であるためUC関連大腸腫瘍に準じて厳密なサーベイランスが必要であると考えられる。一方で非隆起性病変に対して内視鏡的治癒切除がされた場合には,サーベイランスによる経過観察を弱く推奨している8)。この推奨度の違いは非隆起性病変の内視鏡切除術が技術的に困難であることより,再発リスクが高い可能性があることに起因している。内視鏡切除後のサーベイランス法に関するエビデンスは存在しないが,UC関連大腸腫瘍が異時性に発生するリスクが高いことを考慮して,高画素内視鏡を用いてサーベイランスを行い,必要に応じて色素散布や画像強調内視鏡の併用を考慮することが推奨される。
文献
- Iacopini F, Saito Y, Yamada M, et al.:Curative endoscopic submucosal dissection of large nonpolypoid superficial neoplasms in ulcerative colitis(with videos). Gastrointest Endosc 2015;82:734-738
- Suzuki N, Toyonaga T, East JE:Endoscopic submucosal dissection of colitis-related dysplasia. Endoscopy 2017;49:1237-1242
- Kinoshita S, Uraoka T, Nishizawa T, et al.:The role of colorectal endoscopic submucosal dissection in patients with ulcerative colitis. Gastrointest Endosc 2018;87:1079-1084
- Yang DH, Kim J, Song EM, et al.:Outcomes of ulcerative colitis-associated dysplasia patients referred for potential endoscopic submucosal dissection. J Gastroenterol Hepatol 2019;34:1581-1589
- Matsumoto K, Oka S, Tanaka S, et al.:Long-Term Outcomes after Endoscopic Submucosal Dissection for Ulcerative Colitis-Associated Dysplasia. Digestion 2021;102:205-215
- Manta R, Zullo A, Telesca DA, et al.:Endoscopic Submucosal Dissection for Visible Dysplasia Treatment in Ulcerative Colitis Patients:Cases Series and Systematic Review of Literature. J Crohns Colitis 2021;15:165-168
- Wanders LK, Dekker E, Pullens B, et al.:Cancer risk after resection of polypoid dysplasia in patients with longstanding ulcerative colitis:a meta-analysis. Clin Gastroenterol Hepatol 2014;12:756-764
- Laine L, Kaltenbach T, Barkun A, et al.:SCENIC international consensus statement on surveillance and management of dysplasia in inflammatory bowel disease. Gastrointest Endosc 2015;81:489-501. e26
CQ 23:IBD関連消化管癌手術後のIBD薬物治療の注意点は何か?
IBD関連消化管癌手術後の患者において免疫抑制的治療が必要な場合には,癌再発リスクを考慮し,消化器内科医,腫瘍内科医,外科医による議論のうえ,個々の症例に応じて,安全性と有効性を考慮して治療方針を決定する。(エビデンスレベルD)
● 解説
UC術後回腸囊炎に対する治療やCD術後再発に対する予防を目的とし,手術後にも生物学的製剤などの免疫抑制的治療が用いられることがある。
臓器移植後の患者において,チオプリン製剤,カルシニューリン阻害薬のような免疫調節薬の長期使用は,新規の癌発生や癌の再発リスクを上昇させる可能性が報告されている1)。このようなデータから免疫調節薬や生物学的製剤といった免疫抑制的治療は,IBD関連消化管腫瘍術後の癌の再発率を上昇させることが懸念される。
IBD薬物治療がIBD関連消化管癌治療後の癌再発率に影響するかを検証した研究は,後ろ向き研究も含め報告がないものの,癌既往のあるIBD患者において新規の癌発生率および癌再発率について免疫抑制的治療患者と非治療患者を比較した後ろ向き研究は1編見られる2)。本報告は消化管腫瘍,皮膚腫瘍,血液悪性疾患,他の固形腫瘍の既往のあるIBD患者を対象とし,免疫抑制的治療が新規の癌発生および癌再発率に影響しなかったことを報告している(免疫調節薬:HR 1.08(95%信頼区間0.54-2.15),抗TNFα抗体製剤:HR 0.32(95%信頼区間0.09-1.09),抗TNFα抗体製剤・免疫調節薬併用:HR 0.64(95%信頼区間0.26-1.59))。消化管癌治療歴を持つIBD患者における免疫抑制的治療の癌再発率への影響を検討した研究はこれまで報告されていない。
2016年に報告された16編の論文(関節リウマチ9編,IBD 8編,乾癬1編)を対象とした癌既往患者の再発率を検討したメタアナリシスでは,免疫抑制的治療(抗TNFα抗体製剤,免疫調節薬)の新規の癌発生率または癌再発率への影響を検討している3)。本報告では非メラノーマ皮膚癌,乳癌等を含む癌の既往のある患者において,抗TNFα抗体製剤,免疫調節薬,抗TNFα抗体製剤・免疫調節薬の併用は,免疫抑制的治療が行われなかった患者と比較して新規の癌発生率または癌再発率において差がなかったという結果が報告された(免疫調節薬:発生率36.2/1,000 person-years(95%信頼区間17.7-54.7),抗TNFα抗体製剤:発生率33.8/1,000 person-years(95%信頼区間22.3-45.2),抗TNFα抗体製剤・免疫調節薬併用:発生率54.5/1,000 person-years(95%信頼区間29.7-79.3),免疫抑制的治療なし:発生率37.5(95%信頼区間20.2-54.7)。
また同様に2019年に報告された9編の論文(関節リウマチ8編,IBD 2編)を対象とした癌既往患者の再発率を検討したメタアナリシスでは,抗TNFα抗体製剤の新規の癌発生率および癌再発率へ影響は見られなかったと報告している4)(発生率比0.90,95%信頼区間0.59-1.37)。
ウステキヌマブ,ベドリズマブ,トファシチニブの癌既往患者に対する影響を検討したシステマティックレビューおよびメタアナリシスは見られない。腸管に選択的に作用するベドリズマブはその作用機序から最も安全性が高いと考えられている。
長期間の全身性ステロイド使用はリンパ腫や非メラノーマ皮膚癌の発生リスクが高まる可能性が報告されているが5,6),消化管癌治療歴を持つIBD患者における全身性ステロイドの癌再発リスクに関する報告はない。ECCOのガイドライン7)によると癌の既往のある活動性のIBD患者において短期間の全身性ステロイドであれば症例に応じて考慮されると記載されている。5-ASA,栄養療法,局所ステロイド療法は一般的に安全性が高いと考えられている7)。
これまでのメタアナリシスでは癌既往患者における免疫抑制的治療の癌再発率への影響は明らかでなく,癌の既往のあるIBD患者における免疫抑制的治療を一律に禁じるべきではないことを示唆している。一方で,癌再発リスクが上昇することは完全に否定されておらず,ECCOのガイドライン7)では,免疫抑制的治療は癌治療完了後少なくとも2年間,再発リスクが中程度あるいは高い患者では治療完了後5年間は使用しないことが推奨されている。
IBD関連消化管癌手術後の患者においても癌治療が終了した後に免疫抑制的治療を行うことを原則とし,免疫抑制的治療が必要な場合には,癌再発リスクを考慮し,消化器内科医,腫瘍内科医,外科医による議論のうえ,個々の症例に応じて,安全性と有効性を考慮して治療方針を決定することが推奨される。
文献
- Gutierrez-Dalmau A, Campistol JM:Immunosuppressive therapy and malignancy in organ transplant recipients:a systematic review. Drugs 2007;67:1167-1198
- Axelrad J, Bernheim O, Colombel JF, et al.:Risk of New or Recurrent Cancer in Patients With Inflammatory Bowel Disease and Previous Cancer Exposed to Immunosuppressive and Anti-Tumor Necrosis Factor Agents. Clin Gastroenterol Hepatol 2016;14:58-64
- Shelton E, Laharie D, Scott FI, et al.:Cancer Recurrence Following Immune-Suppressive Therapies in Patients With Immune-Mediated Diseases:A Systematic Review and Meta-analysis. Gastroenterology 2016;151:97-109. e104
- Micic D, Komaki Y, Alavanja A, et al.:Risk of Cancer Recurrence Among Individuals Exposed to Antitumor Necrosis Factor Therapy:A Systematic Review and Meta-Analysis of Observational Studies. J Clin Gastroenterol 2019;53:e1-e11
- Jensen AØ, Thomsen HF, Engebjerg MC, et al.:Use of oral glucocorticoids and risk of skin cancer and non-Hodgkin’s lymphoma:a population-based case-control study. Br J Cancer 2009;100:200-205
- Sørensen HT, Mellemkjaer L, Nielsen GL, et al.:Skin cancers and non-hodgkin lymphoma among users of systemic glucocorticoids:a population-based cohort study. J Natl Cancer Inst 2004;96:709-711
- Annese V, Beaugerie L, Egan L, et al.;ECCO:European Evidence-based Consensus:Inflammatory Bowel Disease and Malignancies. J Crohns Colitis 2015;9:945-965
CQ 24:IBD関連消化管腫瘍手術後の補助化学療法は推奨されるか?
IBD関連大腸腫瘍
手術後の補助化学療法について,有効性を判断できない。個々の症例に応じて適否を判断する。(推奨度なし・エビデンスレベルD)
CD関連小腸腫瘍
手術後の補助化学療法について,有効性を判断できない。(推奨度なし・エビデンスレベルD)
● 解説
IBD関連消化管腫瘍治療後に対する補助化学療法の有用性を施行群と非施行群とで比較したランダム化比較試験は存在しない。IBD患者が増加しているとはいえ,本邦でUCが約20万人,CDが約7万人しかおらず,消化管腫瘍が発生するのはその中の一部である。散発性大腸癌の発症人数が年間約10万人を超えていることに比べると,IBD関連消化管腫瘍症例は非常に少ない。さらにIBDの炎症程度や病変の広がり,栄養状態,UCならば大腸全摘術後の身体への影響など個人差が大きいことを勘案すると,前向き観察研究を行うことは大変困難である。
IBD関連大腸腫瘍
IBD関連大腸癌で化学療法を行った報告自体が非常に少ない。米国からUC関連大腸癌27人へ補助化学療法が行われた報告があるが,化学療法の内容や有害事象の記載がなく,化学療法の有無で予後の比較はない1)。IAAが行われた大腸癌82症例をまとめた報告では,化学療法が行われた16人のうち2人が下痢,1人が肝炎で減量または中止となったが,対象症例がUC例だけでなく家族性大腸腺腫症例も含めた結果であった2)。IBD関連大腸癌34例の比較がフランスから報告されており,補助化学療法が15例に行われているものの,レジメン,有害事象は不明である3)。他施設データでIBDの有無で直腸癌の予後を検討した報告(Stageや年齢をそろえた比較)では,IBD関連直腸癌と散発性直腸癌で予後に差はなかったものの,補助化学療法を受けた割合がIBD関連直腸癌で46%(49/107),散発性直腸癌で56%(121/215)とIBD関連直腸癌で低い傾向(p=0.083)にあった4)。しかしIBD関連直腸癌を補助化学療法の有無で比較検討しておらず,補助化学療法の有効性は証明されていない。IBD関連大腸癌29例(UC 18例,CD 11例)の化学療法を検討した報告が本邦から出ており5),うち16例に補助化学療法が行われた(FOLFOX療法2例,CAPOX療法2例,S-1 7例,capecitabine 1例,UFT+LV療法3例,その他1例)。減量を要したのが5例(31%)であり,その原因は血液学的異常50%,疲労17%,手足症候群17%,クレアチニン上昇17%であった。補助化学療法が完遂されたものは44%であり,Grade 3/4の有害事象は好中球減少が19%と最も多くみられた。しかし各レジメンの症例数が非常に少ないことは否めない。ほかにも47歳のCD関連盲腸癌に術後FOLFOX療法を行った症例報告があるが,その予後や有害事象の記載はない6)。
このようにIBD関連大腸腫瘍の補助化学療法については適否を判定する基準はない。現段階では手術後の補助化学療法について,有効性を判断できない,とした。しかしIBD関連大腸腫瘍は若い症例が多く,術後再発のリスクを下げることは重要である。したがって,術後の補助化学療法は,癌のStageや癌再発リスクだけでなくIBD患者の全身状態,栄養状態,年齢,IBDの炎症程度や病変の広がり,IBDの治療内容や治療効果などを考慮して適否を判断する。
CD関連小腸腫瘍
CD関連小腸腫瘍の補助化学療法についての論文はなく,補助化学療法の是非について判断できない。
文献
- Gorfine SR, Harris MT, Bub DS, et al.:Restorative proctocolectomy for ulcerative colitis complicated by colorectal cancer. Dis Colon Rectum 2004;47:1377-1385
- Radice E, Nelson H, Devine RM, et al.:Ileal pouch-anal anastomosis in patients with colorectal cancer:Long-term functional and oncologic outcomes. Dis Colon Rectum 1998;41:11-17
- Ouaïssi M, Maggiori L, Alves A, et al.:Colorectal cancer complicating inflammatory bowel disease:A comparative study of Crohn’s disease vs ulcerative colitis in 34 patients. Colorectal Dis 2011;13:684-688
- Alsughayer A, Grass F, McKenna NP, et al.:Does IBD portend worse outcomes in patients with rectal cancer? A case-matched analysis. Dis Colon Rectum 2020;63:1265-1275
- Nio K, Higashi D, Kumagai H, et al.:Efficacy and safety analysis of chemotherapy for advanced colitis-associated colorectal cancer in Japan. Anticancer Drugs 2016;27:457-463
- Coelho R, Silva M, Gaspar R, et al.:“A book should not be judged by its cover”:two cases of intestinal adenocarcinoma as the first manifestation of Crohn’s disease. Int J Colorectal Dis 2016;31:1061-1062
CQ 25:IBD関連の進行・再発消化管癌に対する薬物療法は推奨されるか?
IBD関連の進行・再発消化管癌に対する薬物療法は,散発性消化管癌に対する薬物療法と同等の有効性は示されていないものの,全身状態が良好でかつ主要臓器機能が保たれている場合に実施することを弱く推奨する。(推奨度2・エビデンスレベルC,合意率: 86%)
● 解説
IBD関連の進行・再発消化管癌に対する薬物療法の目標は,腫瘍の進行を遅延させ,延命と症状コントロールを図ることである。IBD関連の進行・再発消化管癌症例に対する薬物療法の有効性を散発性消化管癌と比較したメタアナリシスやランダム化比較試験,前向きコホート研究は存在せず,本邦ではIBD関連消化管癌の主である大腸癌の治療ガイドライン1)に準じ,全身状態,主要臓器機能を評価し薬物療法の適応判断やレジメン選択が行われているのが現状である。薬物療法の実施にあたっては,胃腸障害や血液障害など有害事象の発現に注意するとともにIBDの活動性についても適宜評価する必要がある。
IBD関連の進行・再発消化管癌に対する薬物療法の有効性
IBD関連の進行・再発消化管癌18例(大腸癌15例,小腸癌3例)を背景,薬物療法レジメンを1:1でマッチさせた散発性消化管癌症例と比較した後ろ向き症例対照研究2)によると,一次治療(FOLFOXまたはFOLFOX+BEV療法9例,FOLFIRIまたはFOLFIRI+BEV療法6例,5FU+l-LV療法3例,FOLFOX+肝動注療法:1例)に対する奏効率は2群間で有意差を認めなかった(35.7% vs. 57.1%,p=0.45)ものの,IBD関連消化管癌群で奏効期間中央値が有意に短く(1.4カ月vs. 11.8カ月,p=0.006),生存期間中央値(MST)も有意に短縮していた(13.5カ月vs. 27.6カ月,p=0.034)。また,IBD関連大腸癌80例(UC 55例,CD 25例)を背景,癌進行度,治療内容(薬物療法レジメン含む)をマッチさせた散発性大腸癌78例と比較した後ろ向き症例対照研究3)においても,Stage Ⅳ症例での5年生存率がIBD関連大腸癌群で有意に低下していた(19% vs. 50%,p=0.017)。本邦では,IBD関連大腸癌29例(UC 18例,CD 11例)を対象とした後ろ向き症例集積研究4)の中で,palliative chemotherapyを施行した13例(FOLFOX療法 6例,FOLFOX+BEV療法3例,その他4例)で,奏効率15%,無増悪生存期間(PFS)中央値182日,MSTが315日であったと報告されている。
なお,IBD関連消化管腫瘍でしばしばみられる大腸粘液癌を対象としたレビュー5)では,palliative chemotherapyの有効性を粘液癌群と非粘液癌群で比較した4つの症例対照研究すべてで粘液癌群のOSが有意に短く,予後不良であったと述べられている。
薬物療法の忍容性と有害事象
前述の後ろ向き症例対照研究3)では,薬物療法の開始遅延や中断,薬剤減量といった治療内容の変更がIBD関連大腸癌症例において有意に多く(74% vs. 44%,p=0.03),主に下痢や腸炎,イレウスなど胃腸障害の影響が指摘されている。Nioら4)も薬物療法に伴うGrade 3/4の有害事象を55%に認め,38%で薬剤の減量を要したとしている。またIBD関連消化管癌8例(UC 3例,CD 5例)を対象に薬物療法の有害事象を検討した後ろ向き症例集積研究6)によると,胃腸障害で最も多いのは下痢(75%)でGrade 3を呈したのは全例CDであり,血液およびリンパ系障害では貧血(75%)が最も多く,次いでリンパ球減少(38%),好中球減少(30%)が挙げられ,Grade 3の好中球減少を25%に認めたと報告されている。
薬物療法とIBDの病勢コントロール
薬物療法施行中は,主要臓器機能保持の点からIBDの病勢がコントロールされていることが望まれる。薬物療法に伴う有害事象とIBDの活動性に関し,Grade 3/4の胃腸障害発現率がIBDの寛解期と比べ活動期で有意に多かった(57% vs. 5%,p<0.01)との報告4)がある。他方,Axelardら3)はIBDの活動性が薬物療法の開始遅延や中断,薬剤減量に影響しなかったとしているが,薬物療法に伴う胃腸障害とIBDの消化器症状の鑑別が時に困難であることに注意が必要である。
抗がん剤の免疫抑制作用によりIBDの病勢がコントロールされうる7-9)との意見もあるが,薬物療法がIBDの病勢に与える影響は未だ明らかでない。ECCO malignancy consensus7)では,5-ASA製剤,栄養療法,局所ステロイド製剤は担癌状態であっても安全に使用できるとされている一方,少なくとも薬物療法施行中はチオプリン製剤,カルシニューリン阻害薬,抗TNFα抗体製剤の投与を避けるよう推奨されている(CQ 23)。ただしIBDの再燃時はその限りでなく,内科医,腫瘍内科医,外科医がそれぞれの専門性をもって治療方針を協議し,症例ごとに判断されることが望ましい。
文献
- 大腸癌研究会編:大腸癌治療ガイドライン医師用2019年版,金原出版,東京,2019
- Yaeger R, Paroder V, Bates DDB, et al.:Systemic chemotherapy for metastatic colitis-associated cancer has a worse outcome than sporadic colorectal cancer:matched case cohort analysis. Clin Colorectal Cancer 2020;19:e151-e156
- Axelrad J, Kriplani A, Ozbek U, et al.:Chemotherapy tolerance and oncologic outcome in patients with colorectal cancer with and without inflammatory bowel disease. Clin Colorectal Cancer 2017;16:e205-e210
- Nio K, Higashi D, Kumagai H, et al.:Efficacy and safety analysis of chemotherapy for advanced colitis-associated colorectal cancer in Japan. Anticancer Drugs 2016;27:457-463
- Luo C, Cen S, Ding G, et al.:Mucinous colorectal adenocarcinoma:clinical pathology and treatment options. Cancer Commun(Lond)2019;39:13
- Naito A, Mizushima T, Takeyama H, et al.:Feasibility of Chemotherapy in Patients with Inflammatory Bowel Disease-Related Gastrointestinal Cancer. Hepatogastroenterology 2014;61:942-946
- Annese V, Beaugerie L, Egan L, et al.:European Evidence-based Consensus:Inflammatory Bowel Disease and Malignancies. J Crohns Colitis 2015;9:945-965
- Goessling W, Mayer RJ:Systemic treatment of patients who have colorectal cancer and inflammatory bowel disease. Gastroenterol Clin North Am 2006;35:713-727
- Jauregui-Amezaga A, Vermeire S, Prenen H:Use of biologics and chemotherapy in patients with inflammatory bowel diseases and cancer. Ann Gastroenterol 2016;29:127-136
CQ 26:IBD関連直腸癌に対する術前化学放射線療法は有効か?
IBD関連直腸癌に対する術前化学放射線療法の有効性と安全性は確立されていない。(推奨度なし・エビデンスレベルC)
● 解説
直腸癌に対する術前化学放射線療法は,欧米を中心にR0切除可能例の全生存率の向上や局所再発率の低下,腫瘍縮小に伴う括約筋温存などを期待して行われてきた。本邦では下部直腸進行癌に対してtotal mesorectal excision(直腸間膜全切除)(あるいはtumor-specific mesorectal excision)+側方郭清が標準治療として行われ,良好な成績が報告されており,術前化学放射線療法の局所再発低減における上乗せ効果,あるいは側方郭清の代替としての有効性については,現時点で明らかなエビデンスはなく,適切に計画された臨床試験での評価が必要であるという理由から,大腸癌治療ガイドラインでは,「局所再発リスクが高い直腸癌の場合は,術前化学放射線療法を行うことを弱く推奨する。(推奨度2・エビデンスレベルB)」とされている。一方,遠隔転移のない切除不能な局所進行直腸癌では,局所効果で全身薬物療法を上回る可能性を考慮して,「腫瘍縮小によりR0切除が可能になると期待される症例に対しては,切除を指向した化学放射線療法を行うことを弱く推奨する。(推奨度2・エビデンスレベルB)」とされている。
しかし,IBD関連直腸癌に限った術前化学放射線療法の報告は限られており,化学放射線療法の有効性と併存するIBDの病態や実施する手術の安全性を考慮して実施を検討する必要がある。
術前化学放射線療法は安全に実施できるとの報告は多い1-3)。CD患者に合併する痔瘻癌に対する実施例も報告されている4-6)。一方で,UC患者の腸管に対する放射線照射は正常腸管に対する照射より副作用が多い7)という報告や化学放射線療法中にIBDの増悪を来したとの報告もあり,通常の直腸癌に対する化学放射線療法以上の注意が必要である。
化学放射線療法後の手術に関しては,会陰創関連合併症,治癒遅延との関連が報告されているがIBD関連直腸癌に特有のものではなく8),合併症リスクが増加するという報告はない。術前化学放射線療法の施行により慢性回腸囊炎や回腸囊不全発生率は高くなる9,10)との報告があり,IAA前の骨盤内放射線照射は術後の機能不良につながると考えられている11)。
有効性に関しては通常の直腸癌と同程度と考えられているが12),IBD関連直腸癌で全生存率の向上や局所再発率の低下を示した報告はない。通常の直腸癌と比較してIBD関連直腸癌では術前化学放射線療法の施行率が有意に低く,CRM陽性率が有意に高いこと,IBD関連直腸癌の全生存率,無再発生存率が低い傾向であることの報告があるが13),まだ十分なデータがあるとはいえず,有効性と安全性は確立していない。
文献
- Bosch SL, van Rooijen SJ, Bökkerink GM, et al.:Acute toxicity and surgical complications after preoperative(chemo)radiation therapy for rectal cancer in patients with inflammatory bowel disease. Radiother Oncol 2017;123:147-153
- 池内浩基,内野 基,松岡宏樹,他:クローン病直腸肛門部における癌合併.IBD Res 2010;4:107-112
- 荒木俊光,井上靖浩,田中光司,他:潰瘍性大腸炎に合併した直腸・肛門管癌の外科治療.日臨2012;70(Suppl 1):535-540
- 木ノ下 修,中西正芳,村山康利,他:術前化学放射線療法により切除可能となったCrohn病に合併した局所進行痔瘻癌の1例.日消外会誌2013;46:463-470
- Iesalnieks I, Gaertner WB, Glass H, et al.:Fistula-associated anal adenocarcinoma in Crohn’s disease. Inflamm Bowel Dis 2010;16:1643-1648
- Scharl M, Frei P, Frei SM, et al.:Epithelial-to-mesenchymal transition in a fistula-associated anal adenocarcinoma in a patient with long-standing Crohn’s disease. Eur J Gastroenterol Hepatol 2014;26:114-118
- Green S, Stock RG, Greenstein AJ:Rectal cancer and inflammatory bowel disease:natural history and implications for radiation therapy. Int J Radiat Oncol Biol Phys 1999;44:835-840
- Althumairi AA, Canner JK, Gearhart SL, et al.:Predictors of Perineal Wound Complications and Prolonged Time to Perineal Wound Healing After Abdominoperineal Resection. World J Surg 2016;40:1755-1762
- Radice E, Nelson H, Devine RM, et al.:Ileal pouch-anal anastomosis in patients with colorectal cancer:long-term functional and oncologic outcomes. Dis Colon Rectum 1998;41:11-17
- Hultén L:Conversion of a pelvic pouch to a continent pouch(Kock pouch). Tech Coloproctol 2001;5:192
- Wu XR, Kiran RP, Remzi FH, et al.:Preoperative pelvic radiation increases the risk for ileal pouch failure in patients with colitis-associated colorectal cancer. J Crohns Colitis 2013;7:e419-e426
- Ali RA, Dooley C, Comber H, et al.:Clinical features, treatment, and survival of patients with colorectal cancer with or without inflammatory bowel disease. Clin Gastroenterol Hepatol 2011;9:584-589.e1-2
- Alsughayer A, Grass F, McKenna NP, et al.:Does IBD Portend Worse Outcomes in Patients with Rectal Cancer? A Case-Matched Analysis. Dis Colon Rectum 2020;63:1265-1275
CQ 27:IBD関連消化管癌は散発性消化管癌と比較して予後不良か?
IBD関連大腸癌
IBD関連大腸癌は散発性大腸癌と比較して予後が不良である。(エビデンスレベルB)
CD関連小腸癌
CD関連小腸癌は予後不良であるが,散発性小腸癌とは発生部位の頻度も異なり両者の予後の直接比較は困難である。(エビデンスレベルC)
● 解説
IBD関連大腸癌と散発性大腸癌の予後を比較したメタアナリシスが2016年,2017年および2021年に報告されている1-3)。2016年のメタアナリシス(12編)ではIBD関連大腸癌が散発性大腸癌より予後不良1),2017年のメタアナリシス(13編)では予後は同等と結論され2),一定の見解は得られていなかった。2021年のメタアナリシスではIBD全体で25編の研究が統合され,IBD関連大腸癌の予後が不良であることが示され(HR 1.33,95%信頼区間1.20-1.40),UC関連大腸癌とCD関連大腸癌に分けて解析しても散発性大腸癌よりも予後が悪いことが示された3)。
2020年に出版されたスウェーデンとデンマークの10万人弱の大規模なコホート研究ではIBD関連大腸癌は散発性大腸癌よりも発見されるStageがより早期であるにもかかわらず生存率が低いという報告がなされている4)。
また,IBD関連大腸癌は散発性大腸癌と比べてsignet ring cellなどの悪性度が高いものが多いとされており,散発性大腸腫瘍ではAPC等の変異が早期に起こりTP53の変異は遅い段階で起こるのに対し,IBD関連大腸腫瘍では比較的早期にTP53の変異が起こり,APCの変異の頻度は低く遅い段階で起こるなど,この両者には遺伝子変異の違いがあると考えられている5)。今後,がんゲノム医療の進歩とともにIBD関連消化管癌の予後も改善していく可能性が期待される。
UC関連大腸癌
UC関連大腸癌は散発性消化管癌と比較して予後が不良である。2021年のメタアナリシスにおけるUC関連大腸癌と散発性大腸癌の比較では,10編の論文が統合解析され,HRは1.35(95%信頼区間1.16-1.57)でUC関連大腸癌の予後が不良であった3)。本邦多施設からのUC関連大腸癌238例の症例解析における5年生存率はStage Ⅰ 93.9%,Stage Ⅱ 90.7%,Stage Ⅲ 62.2%(Ⅲa 76.8%,Ⅲb 38.0%,Ⅲc 29.6%),Stage Ⅳ 8.4%と報告されている6)。
大腸癌の生存率はStageにより異なるが,Stage ⅢやStage Ⅳ大腸癌の5年生存率は補助化学療法や分子標的治療薬の開発とともに向上している。また人種により大腸癌の生存率が異なる可能性も指摘されている。そのような観点からIBD関連消化管癌と散発性消化管癌の予後の比較においては,日本人において同時期に同じコホートで癌のStage別に比較をすることも重要である。本邦の大腸癌研究会による研究ではUC関連大腸癌と散発性大腸癌をStage別に比較した結果,Stage ⅢにおいてUC関連大腸癌の方が散発性大腸癌よりも予後が悪いと結論づけられている(Stage Ⅲの5年生存率:UC関連大腸癌43.3%,散発性大腸癌57.4%,p=0.0320)7)。
CD関連消化管癌
CD関連大腸癌は散発性消化管癌と比較して予後が不良である。CD関連小腸癌は予後不良であるが,散発性小腸癌とは発生部位の頻度も異なり両者の予後の直接比較は困難である。2021年のメタアナリシスにおけるCD関連大腸癌と散発性大腸癌の比較では,5編の論文が統合されているが,すべての論文でCD関連大腸癌の予後不良が有意に示されており,統合解析の結果HRは1.32(95%信頼区間1.24-1.40)でCD関連大腸癌の予後が不良であった3)。このメタアナリシスには本邦の論文は含まれていないが,本邦の単施設のコホート研究において,CDでは一般集団と比較して大腸癌の標準化死亡比(standardized mortality ratio:SMR)が29.7(95%信頼区間16.5-53.7)であることが示されており,大腸癌による死亡率がCD集団では一般集団よりも高いことが示唆されている8)。本邦多施設からのCD関連消化管癌の症例解析でも一般集団との比較ではないが予後が不良であることが報告されている9,10)。本邦多施設の122例(小腸癌10%,肛門管癌51%を含む)のうち解析可能症例119例における5年生存率はStage Ⅰ 88%,Stage Ⅱ 68%,Stage Ⅲa 71%,Stage Ⅲb 25%,Stage Ⅳ 0%と報告されている10)。
CD関連消化管癌は小腸・大腸・肛門と広い範囲の消化管および瘻孔に発生しうる。欧米では散発性消化管癌と比較し右側結腸癌の比率が高く(CQ 3),大腸内視鏡検査によるサーベイランスが推奨されている。本邦における発生部位は痔瘻を含めた直腸肛門部に多いことが知られており,欧米とは分布が異なっている9)。CDに関連する直腸肛門管癌や小腸癌は早期発見が難しく,IBD関連消化管癌だけに限ったことではないがその予後が不良である症例が多い9)。直腸肛門管癌に対しては欧米で推奨される内視鏡的サーベイランスに加えて麻酔下に直腸肛門部の生検を行うことで早期発見を目指す試みが本邦の専門施設を中心に行われている(CQ 9)。
2022年のメタアナリシス(CD関連小腸癌879例の統合解析)ではCD関連小腸癌の5年全生存率は29%(95%信頼区間0.18-0.41)と不良であることが報告されている11)。このメタアナリシスではCD関連小腸癌と散発性小腸癌の予後の比較もなされているが,統合された論文のすべてが散発性小腸癌のコホートを含んでいるわけではないことや十二指腸癌も含まれていることからこの解析の結論は限定的である。このメタアナリシスにも含まれているアメリカ合衆国のNational Cancer Databaseからの十二指腸癌を除いた小腸癌コホート(CD関連小腸癌493例,散発性小腸癌2,175例)の解析では,5年全生存率はCD関連小腸癌41.1%,散発性小腸癌35.4%(p=0.09)と報告されており,Stage別の解析でも両者の生存率に統計学的有意差はみられなかった12)。CD関連小腸癌は回腸に多いのに対し,散発性小腸癌は十二指腸や空腸に多いことも両者の予後を直接比較し断定的な結論を得ることを困難にしている要素の一つである。
文献
- Reynolds IS, O’Toole A, Deasy J, et al.:A meta-analysis of the clinicopathological characteristics and survival outcomes of inflammatory bowel disease associated colorectal cancer. Int J Colorectal Dis 2017;32:443-451
- Ou B, Zhao J, Guan S, et al.:Survival of Colorectal Cancer in Patients With or Without Inflammatory Bowel Disease:A Meta-Analysis. Dig Dis Sci 2016;61:881-889
- Lu C, Schardey J, Zhang T, et al.:Survival Outcomes and Clinicopathological Features in Inflammatory Bowel Disease-Associated Colorectal Cancer:A Systematic Review and Meta-Analysis. Ann Surg 2022;276:e319-e330
- Olen O, Erichsen R, Sachs MC, et al.:Colorectal cancer in ulcerative colitis:a Scandinavian population-based cohort study. Lancet 2020;395:123-131
- Svrcek M, Borralho Nunes P, Villanacci V, et al.:Clinicopathological and Molecular Specificities of Inflammatory Bowel Disease-Related Colorectal Neoplastic Lesions:The Role of Inflammation. J Crohns Colitis 2018;12:1486-1498
- Hata K, Anzai H, Ikeuchi H, et al.;Research Group for Intractable Inflammatory Bowel Disease of the Ministry of Health, Labour and Welfare of Japan(RGIBD):Surveillance Colonoscopy for Ulcerative Colitis-Associated Colorectal Cancer Offers Better Overall Survival in Real-World Surgically Resected Cases. Am J Gastroenterol 2019;114:483-489
- Watanabe T, Konishi T, Kishimoto J, et al.;Japanese Society for Cancer of the Colon and Rectum:Ulcerative colitis-associated colorectal cancer shows a poorer survival than sporadic colorectal cancer:a nationwide Japanese study. Inflamm Bowel Dis 2011;17:802-808
- Yasukawa S, Matsui T, Yano Y, et al.:Crohn’s disease-specific mortality:a 30-year cohort study at a tertiary referral center in Japan. J Gastroenterol 2019;54:42-52. Erratum in:J Gastroenterol 2021;56:1111-1112
- 篠崎 大:クローン病と下部消化管癌―本邦の現況―.日本大腸肛門病会誌2008;61:353-363
- Higashi D, Katsuno H, Kimura H, et al.:Current State of and Problems Related to Cancer of the Intestinal Tract Associated with Crohn’s Disease in Japan. Anticancer Res 2016;36:3761-3766
- Chin, YH, Jain, SR, Lee, MH, et al.:Small bowel adenocarcinoma in Crohn’s disease:a systematic review and meta-analysis of the prevalence, manifestation, histopathology, and outcomes. Int J Colorectal Dis 2022;37:239-250
- Fields AC, Hu FY, Lu P, et al.:Small bowel adenocarcinoma:is there a difference in survival for Crohn’s versus sporadic cases? J Crohns Colitis 2020;14:303-308
CQ 28:IBD患者に消化管以外の腫瘍発生リスクはあるか?
- IBD患者における腸管外悪性腫瘍全体の発生リスクは一般集団と比較して有意に上昇する。(エビデンスレベルB)
- IBD患者では肝胆道癌,血液悪性腫瘍,皮膚癌(非悪性黒色腫皮膚癌(nonmelanoma skin cancer:NMSC),悪性黒色腫)の発生リスクが増加する。(エビデンスレベルB)
● 解説
IBD患者における消化管以外の腫瘍発生リスクについては,集団ベースのコホート研究をまとめた2つのシステマティックレビューが報告されている1,2)。2009年までに報告された8件のコホート研究をまとめたPedersenらのメタアナリシスでは,IBD患者における腸管外悪性腫瘍の全体的な発生リスクは一般集団と比べ同等であった(標準化罹患比(standard incidence ratio:SIR)1.10,95%信頼区間0.96-1.27)1)。一方,2020年までに報告された15件の集団ベースのコホート研究をまとめたLoらのメタアナリシスでは,IBD患者における腸管外悪性腫瘍の全体的な発生リスクは,CD(罹患率比(incidence rate ratio:IRR)1.43,95%信頼区間1.26-1.63)およびUC(IRR 1.15,95%信頼区間1.02-1.31)のいずれにおいても一般集団と比較して有意に上昇することが報告されている2)。また個別の悪性腫瘍の発生リスクに関しては,肝胆道癌,血液悪性腫瘍,皮膚癌(NMSC,悪性黒色腫),肺癌で発生リスクの増加が示されている2)。
IBD患者における胆道癌の発生リスクはUC(IRR 2.93,95%信頼区間1.73-4.98),CD(IRR 2.93,95%信頼区間1.16-7.41)のいずれでも有意に上昇する2)。胆道癌発生に関連するリスク因子としては若年発症,男性,長期罹患歴,PSCの合併などが個々のコホート研究で指摘されている。特にPSC合併例では胆道癌(HR 28.46),肝細胞癌(HR 21.00),膵癌(HR 5.26),胆囊癌(HR 9.19)のいずれの悪性腫瘍についても発生リスクが上昇する3)。
血液悪性腫瘍,特にリンパ腫の発生リスクについてはCD患者で有意に上昇するが(血液悪性腫瘍全体:IRR 2.40,95%信頼区間1.81-3.18,リンパ腫:IRR 1.86,95%信頼区間1.04-3.32),UC患者では発生リスクの増加は認めていない2)。CDおよびUC患者のいずれにおいても特定の血液悪性腫瘍の発生リスク増加は認められない。しかし,CD患者では非ホジキンリンパ腫の発生リスクが高く,チオプリン製剤使用との関連が報告されている4-7)。一方,日本のIBD患者75,673名のDiagnosis Procedure Combination(DPC)データベースを用いた検討ではチオプリン製剤によるリンパ腫の発生率の上昇は認められていない8)。
NMSCについてはCD,UCのいずれにおいても発生リスクが増加するとの報告が多く,メタアナリシスでも同様の結果が示されている(CD:IRR 2.28,95%信頼区間1.36-3.81,UC:IRR 1.36,95%信頼区間1.05-1.77)2)。NMSCのリスク因子としては,特に免疫調節薬の使用がNMSCの発生リスクを増加させるとする報告がある8-10)。しかし,日本人におけるNMSCの発生率は欧米人に比べて低く,チオプリン製剤の使用にあたってはリスク・ベネフィットを十分勘案して判断する8)。一方,悪性黒色腫の発生リスクについてはCD患者でのみ増加する(IRR 1.52,95%信頼区間1.03-2.23)という報告と2),UCおよびCDのいずれにおいても増加するとする2つのメタアナリシスの結果があり11),今後,大規模なサンプルサイズでの検討が必要である。悪性黒色腫の発生に関連するリスク因子として抗TNFα抗体製剤の使用が報告されており12),ECCOのガイドラインでも悪性黒色腫の既往歴のあるIBD患者では抗TNFα抗体製剤の使用を回避することが推奨されている13)。
肺癌の発生リスクについてはLoらのメタアナリシスでCD患者におけるリスク増加が示されている(IRR 1.53,95%信頼区間1.23-1.91)2)。しかしながら,システマティックレビューの対象となった16件のコホート研究のうち,CD患者における肺癌のリスク上昇を示したのは2件のみであり,慎重に解釈する必要がある。腎・尿路系および生殖器系(子宮頸部・体部,卵巣,乳腺,前立腺)についてはメタアナリシスの結果,各臓器における悪性腫瘍の発生リスクの増加は認められていない2)。
文献
- Pedersen N, Duricova D, Elkjaer M, et al.:Risk of extra-intestinal cancer in inflammatory bowel disease:meta-analysis of population-based cohort studies. Am J Gastroenterol 2010;105:1480-1487
- Lo B, Zhao M, Vind I, et al.:The Risk of Extraintestinal Cancer in Inflammatory Bowel Disease:A Systematic Review and Meta-analysis of Population-based Cohort Studies. Clin Gastroenterol Hepatol 2021;19:1117-1138.e19
- Trivedi PJ, Crothers H, Mytton J, et al.:Effects of Primary Sclerosing Cholangitis on Risks of Cancer and Death in People With Inflammatory Bowel Disease, Based on Sex, Race, and Age. Gastroenterology 2020;159:915-928
- Askling J, Brandt L, Lapidus A, et al.:Risk of haematopoietic cancer in patients with inflammatory bowel disease. Gut 2005;54:617-622
- Armstrong RG, West J, Card TR. Risk of cancer in inflammatory bowel disease treated with azathioprine:a UK population-based case-control study. Am J Gastroenterol 2010;105:1604-1609
- Beaugerie L, Brousse N, Bouvier AM, et al.:Lymphoproliferative disorders in patients receiving thiopurines for inflammatory bowel disease:a prospective observational cohort study. Lancet 2009;374:1617-1625
- Lemaitre M, Kirchgesner J, Rudnichi A, et al.:Association Between Use of Thiopurines or Tumor Necrosis Factor Antagonists Alone or in Combination and Risk of Lymphoma in Patients With Inflammatory Bowel Disease. JAMA 2017;318:1679-1686
- Kobayashi T, Uda A, Udagawa E, et al.:Lack of Increased Risk of Lymphoma by Thiopurines or Biologics in Japanese Patients with Inflammatory Bowel Disease:A Large-Scale Administrative Database Analysis. J Crohns Colitis 2020;14:617-623
- van den Heuvel TR, Wintjens DS, Jeuring SF, et al.:Inflammatory bowel disease, cancer and medication:Cancer risk in the Dutch population-based IBDSL cohort. Int J Cancer 2016;139:1270-1280
- Yadav S, Singh S, Harmsen WS, et al.:Effect of Medications on Risk of Cancer in Patients With Inflammatory Bowel Diseases:A Population-Based Cohort Study from Olmsted County, Minnesota. Mayo Clin Proc 2015;90:738-746
- Singh S, Nagpal SJ, Murad MH, et al.:Inflammatory bowel disease is associated with an increased risk of melanoma:a systematic review and meta-analysis. Clin Gastroenterol Hepatol 2014;12:210-218
- Long MD, Martin CF, Pipkin CA, et al.:Risk of melanoma and nonmelanoma skin cancer among patients with inflammatory bowel disease. Gastroenterology 2012;143:390-399.e1
- Annese V, Beaugerie L, Egan L, et al.;ECCO:European Evidence-based Consensus:Inflammatory Bowel Disease and Malignancies. J Crohns Colitis 2015;9:945-965









